

| A. | ①③ | B. | ①④ | C. | ②③ | D. | ②④ |
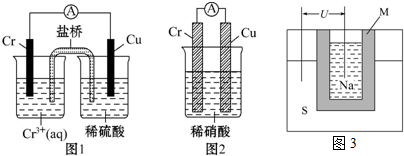
分析 ①图甲:Ag与Cu2+不反应;
②图甲:Cu与Ag+发生置换反应生成Ag;
③图乙中K1闭合,K2断开:形成原电池,Cu为负极,Ag为正极;
④图乙中K1断开,K2闭合:形成电解池,Cu为阳极,失电子生成铜离子,Ag为阴极,阴极上银离子得电子.
解答 解:①图甲:Ag与Cu2+不反应,所以不能发生反应,故错误;
②图甲:Cu与Ag+发生置换反应生成Ag,则发生的反应为:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s),故正确;
③图乙中K1闭合,K2断开:形成原电池,Cu为负极,Ag为正极,发生的电池反应为:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s),故错误;
④图乙中K1断开,K2闭合:形成电解池,Cu为阳极,失电子生成铜离子,Ag为阴极,阴极上银离子得电子,电解反应为:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s),故正确;
故选D.
点评 本题考查原电池和电解池的设计及工作原理,注意电极反应式的书写方法,牢固掌握原电池中电极的判断,电极反应式的书写的方法等问题,题目难度不大.


 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:高中化学 来源: 题型:选择题
| A. | 被氧化的元素与被还原的元素质量比为1:1 | |
| B. | NaBH4是氧化剂,H2O是还原剂 | |
| C. | 硼元素被氧化,氢元素被还原 | |
| D. | NaBH4即使氧化剂又是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2014年1月,国家首次将雾霾天气纳入自然灾情进行通报,雾霾是一种不同于胶体的分散系,它的形成与大量焚烧田间秸秆有关 | |
| B. | 纤维素和淀粉一样可水解成葡萄糖,因此人类可从中获得生存所需的能量 | |
| C. | 2015年诺贝尔化学奖授予从分子水平揭示细胞如何修复损伤DNA以及保护遗传信息的三位科学家,DNA水解产物为氨基酸 | |
| D. | 陶瓷刀号称贵族刀,作为现代高科技的产物,大多是用一种纳米材料“氧化锆”为原料加工而成,具有硬度高、导热性好、抗腐蚀等优点 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
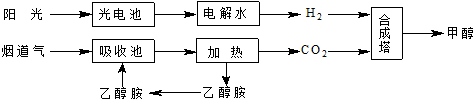
| 反应时间/min | 3 | 5 | 7 | 10 | 13 |
| c(CO2)/mol•L-1 | 0.50 | 0.37 | 0.30 | 0.25 | 0.25 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
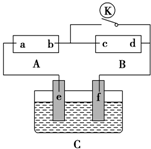 如图所示,A为直流电源,B为浸透饱和硫酸钠溶液和紫色石蕊溶液的滤纸,C为电镀池,接通电路后,发现B上的c点显蓝色,请填空:
如图所示,A为直流电源,B为浸透饱和硫酸钠溶液和紫色石蕊溶液的滤纸,C为电镀池,接通电路后,发现B上的c点显蓝色,请填空:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 澄清的石灰水与稀盐酸反应 Ca (OH)2+2H+═Ca2++2H2O | |
| C. | 酸性溶液中KIO3与KI反应生成I2:IO3-+I-+6H+═I2+3H2O | |
| D. | NaHCO3溶液中加足量Ba(OH)2溶液:HCO3-+Ba2++OH-═BaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com