
【题目】电解原理和原电池原理是电化学的两个重要内容.某兴趣小组做如图探究实验:
(1)如图1为某实验小组依据氧化还原反应设计的原电池装置,若盐桥中装有饱和的KNO3溶液和琼胶制成的胶冻,则NO3﹣移向装置(填写“甲或乙”).其他条件不变,若将CuCl2溶液换为NH4Cl溶液,发现生成无色无味的单质气体,则石墨上电极反应式 . 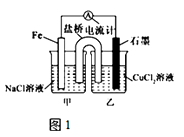
(2)如图2,其他条件不变,若将盐桥换成弯铜导线与石墨相连成n型,则甲装置是(填“原电池或电解池”),乙装置中石墨(2)为极,乙装置中与铁线相连的石墨(1)电极上发生的反应式为 . 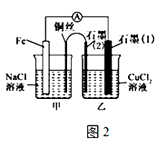
(3)在图2乙装置中改为加入CuSO4溶液,一段时间后,若某一电极质量增重 1.28g,则另一电极生成mL(标况下)气体.
【答案】
(1)甲;2H++2e﹣=H2↑
(2)原电池;阳;Cu2++2e﹣=Cu
(3)224
【解析】解:(1)如图1为原电池装置,铁为负极,阴离子硝酸根向负极移动,所以NO3﹣移向甲移动;正极是氢离子放电生成氢气,电极反应式为:2H++2e﹣=H2↑,所以答案是:甲; 2H++2e﹣=H2↑;(2)其他条件不变,若将盐桥换成弯铜导线与石墨相连成n型,则甲装置是活泼金属发生自发的氧化还原反,是原电池;乙装置中石墨(2)与电池的正极相连是阳极,乙装置中与铁线相连的石墨(1)电极是阴极,发生还原反应,电极反应式为:Cu2++2e﹣=Cu,所以答案是:原电池; 阳; Cu2++2e﹣=Cu;(3)在图2乙装置中改为加入CuSO4溶液,一段时间后,若某一电极质量增重 1.28g,即生成铜 1.28g,物质的量为:0.02mol,所以另一极析出氧气的物质的量为:0.01mol,所以另一电极生成224mL(标况下)气体,所以答案是:224.


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
【题目】常温下,把铁片放入下列溶液中,铁片溶解且固体的总质量减小,并伴有气体产生,则该溶液是(相对原子质量:H-1 Na-23 Fe-56 Cu-64 Ag-108) ( )
A.硅酸钠B.硫酸铜C.稀硫酸D.浓硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲配制5OOmL2mol/L的盐酸,需要36.5%的浓盐酸(密度约为1.2g·cm-3)的体积为
A. 27.4mL B. 83.3mL C. 120mL D. 无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠硫电池作为一种新型储能电池,其应用逐渐得到重视和发展.
(1)Al(NO3)3是制备钠硫电池部件的原料之一.由于Al(NO3)3容易吸收环境中的水分,因此需要对其进行定量分析.具体步骤如图所示: 
①加入过量氨水后发生反应的离子方程式为: .
②操作b为:
③Al(NO3)3待测液中,c(Al3+)=mol/L(用含m、V的代数式表示).
(2)钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2SX)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图1所示: 
物质 | Na | S | Al2O3 |
熔点/℃ | 97.8 | 115 | 2050、 |
沸点/℃ | 892 | 444.6 | 2980 |
①根据表数据,请你判断该电池工作的适宜应控制在(填字母)范围内.
A.100℃以下 B.100~300℃C.300~350℃D.350~2050℃
②放电时,电极A为极,电极B发生反应(填“氧化或还原”)
③充电时,总反应为Na2SX═2Na+xS(3<x<5),则阳极的电极反应式为: .
(3)若把钠硫电池作为电源,电解槽内装有KI及淀粉溶液如图2所示,槽内的中间用阴离子交换膜隔开.通电一段时间后,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅.则右侧发生的电极方程式:;试分析左侧溶液蓝色逐渐变浅的可能原因是: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列常见物质的俗名与化学式对应正确的是
A.水煤气-CH4B.明矾-KAl(SO4)2·12H2O
C.水玻璃-H2SiO3D.纯碱-NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图.反应中镁和铝的关系说法正确的是( )
A.物质的量之比为3:2
B.质量之比为3:4
C.摩尔质量之比为9:8
D.体积之比为2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在同温同压下,下列各组热化学方程式中,△H2>△H1的是( )
A.H2 (g)+Cl2(g)═2HCl(g);△H1 ![]() H2(g)+
H2(g)+ ![]() Cl2(g)═HCl(g);△H2
Cl2(g)═HCl(g);△H2
B.2H2(g)+O2 (g)═2H2O(g);△H1 2H2 (g)+O2 (g)═2H2O(l);△H2
C.CO(g)+ ![]() O2(g)═CO2(g);△H1 2CO(g)+O2(g)═2CO2(g);△H2
O2(g)═CO2(g);△H1 2CO(g)+O2(g)═2CO2(g);△H2
D.S(s)+O2(g)═SO2 (g);△H1 S(g)+O2(g)═SO2 (g);△H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏伽德罗常数的值.下列说法正确的是( )
①1.0L1.0mo1L﹣1的NaAlO2水溶液中含有的氧原子数为2NA
②过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA
③密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA
④.235g核素 ![]() U发生裂变反应:
U发生裂变反应: ![]() U+
U+ ![]() n
n ![]()
![]() Sr+
Sr+ ![]() Xe+10
Xe+10 ![]() n,净产生的中子(
n,净产生的中子( ![]() n)数为10NA
n)数为10NA
⑤氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA
⑥铜粉溶于1L0.5mol/L稀硝酸中,当生成标况下2.24LNO时,溶液中的氮原子数为0.4NA个
⑦标准状况下,11.2升氯气溶于水,转移电子数为0.5NA
⑧12g石墨和C60的混合物中质子总数一定为6NA
⑨25℃时,1L molL﹣1FeCl3溶液中含有0.1NA个Fe(OH)3胶体粒子.
A.②⑥⑧
B.①②⑥
C.③⑦⑧
D.①⑤⑨
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com