
| ²ā¶ØŹ±¼ä/h | 0 | 1 | 2 | 3 | 4 |
| pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
·ÖĪö £Ø1£©ĄūÓĆŃõ»Æ»¹Ō·“Ó¦Ą“·ÖĪö£¬ŃĒĮņĖįŅ×±»Ńõ»Æ£»
£Ø2£©Ćŗ”¢ŹÆÓĶČ¼ÉÕŹ±ÄÜÉś³É“óĮæµÄ¶žŃõ»ÆĮņ”¢µŖŃõ»ÆĪļµČĪļÖŹ£¬ÕāŠ©ĪļÖŹČÜÓŚĖ®ÄÜÉś³ÉĻŌĖįŠŌµÄĪļÖŹ£¬µ±“ļµ½“ļµ½Ņ»¶Ø³Ģ¶ČŹ±¾ĶŠĪ³ÉĖįÓź£¬£»
£Ø3£©ĘÆ°×·ŪµÄÓŠŠ§³É·ÖŹĒ“ĪĀČĖįøĘ£¬Óė¶žŃõ»ÆĢ¼Ė®·“Ӧɜ³É“ĪĀČĖį£®
½ā“š ½ā£ŗ£Ø1£©ŅņŃĒĮņĖįŅ×±»Ńõ»ÆÉś³ÉĮņĖį£¬ĖįŠŌŌöĒ棬ĖłŅŌpH¼õŠ”£¬·¢ÉśµÄ·“Ó¦·½³ĢŹ½ĪŖ£ŗ2H2SO3+O2=2H2SO4»ņ2SO2+2H2O+O2=2H2SO4£¬
¹Ź“š°øĪŖ£ŗ2H2SO3+O2=2H2SO4»ņ2SO2+2H2O+O2=2H2SO4£»
£Ø2£©¢ŁÉŁÓĆĆŗ×÷Č¼ĮĻ”¢¢ŪČ¼ĮĻĶŃĮņ”¢¢ŻæŖ·¢ŠĀÄÜŌ“¶¼Äܹ»¼õÉŁ¶žŃõ»ÆĮņµÄÅÅ·Å£¬ŹĒ¼õÉŁĖįÓź²śÉśµÄÓŠŠ§“ėŹ©£¬¶ų¢Ś¼Ó“óŹÆÓĶ”¢ĆŗĢæµÄæŖ²ÉĖŁ¶Č£¬Ōö¼Ó»ÆŹÆČ¼ĮĻµÄ¹©Ó¦Į棬»įŌö¼Ó¶žŃõ»ÆĮņµÄÅÅ·ÅĮæ£¬ČŻŅ×¼ÓÖŲĖįÓźµÄŠĪ³É£¬¶ų¢ÜŌŚŅŃĖį»ÆµÄĶĮČĄÖŠ¼ÓČėŹÆ»Ņ£¬ŹĒÖĪĄķĶĮČĄĖį»Æ£¬ÓėĖįÓźµÄĪŽ¹Ų£¬
¹Ź“š°øĪŖ£ŗB£»
£Ø3£©ĘÆ°×·ŪÖŠµÄ“ĪĀČĖįøĘÓėæÕĘųÖŠµÄ¶žŃõ»ÆĢ¼¼°Ė®·¢Éś·“Ó¦£¬Éś³ÉĢ¼ĖįøĘŗĶ“ĪĀČĖį£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗCa£ØClO£©2+CO2+H2OØTCaCO3+2HClO£»
¹Ź“š°øĪŖ£ŗCa£ØClO£©2+CO2+H2OØTCaCO3+2HClO£®
µćĘĄ ±¾Ģāæ¼²éĮĖ¶žŃõ»ÆĮņµÄĪŪČ¾¼°ÖĪĄķ”¢ĘÆ°×·ŪµÄ×é³É¼°ŠŌÖŹ£¬ĢāÄæÄѶČÖŠµČ£¬Ć÷Č·³£¼ūĪļÖŹµÄŠŌÖŹĪŖ½ā“š¹Ų¼ü£¬×¢ŅāÕĘĪÕĘÆ°×·ŪµÄĘÆ°×ŌĄķ¼°¶žŃõ»ÆĮņµÄÖĪĄķ·½·Ø£¬ŹŌĢāÅąŃųĮĖѧɜĮé»īÓ¦ÓĆ»ł“”ÖŖŹ¶µÄÄÜĮ¦£®


 ʷѧĖ«ÓžķĻµĮŠ“š°ø
ʷѧĖ«ÓžķĻµĮŠ“š°ø Š”ѧʌĩ³å“Ģ100·ÖĻµĮŠ“š°ø
Š”ѧʌĩ³å“Ģ100·ÖĻµĮŠ“š°ø ĘŚÄ©ø“Ļ°¼ģ²āĻµĮŠ“š°ø
ĘŚÄ©ø“Ļ°¼ģ²āĻµĮŠ“š°ø ³¬ÄÜѧµäµ„ŌŖĘŚÖŠĘŚÄ©×ØĢā³å“Ģ100·ÖĻµĮŠ“š°ø
³¬ÄÜѧµäµ„ŌŖĘŚÖŠĘŚÄ©×ØĢā³å“Ģ100·ÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ijĪŽÉ«ČÜŅŗÖŠ£ŗAl3+”¢Cu2+”¢SO42-”¢Cl- | |
| B£® | ÓÉĖ®µēĄėµÄc£ØH+£©=1”Į10-12 mol•L-1µÄČÜŅŗÖŠ£ŗFe2+”¢K+”¢Cl-”¢NO3- | |
| C£® | $\frac{c£Ø{H}^{+}£©}{c£ØO{H}^{-}£©}$=1012µÄČÜŅŗÖŠ£ŗNa+”¢Mg2+”¢NO3-”¢Cl- | |
| D£® | ŗ¬ÓŠ“óĮæHCO3-µÄČÜŅŗÖŠ£ŗNH4+”¢Al3+”¢Ca2+”¢Cl- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 0.4”÷H1+0.05”÷H3 | B£® | 0.4”÷H1+0.05”÷H2 | C£® | 0.4”÷H1+0.1”÷H3 | D£® | 0.4”÷H1+0.2”÷H3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Li”¢C”¢OŌ×Ó×īĶā²ćµē×ÓŹżŅĄ“ĪŌö¼Ó | B£® | P”¢S”¢ClŌŖĖŲ×īøßÕż»ÆŗĻ¼ŪŅĄ“ĪÉżøß | ||
| C£® | N”¢O”¢FŌ×Ó°ė¾¶ŅĄ“ĪŌö“ó | D£® | Li”¢Na”¢KµÄ½šŹōŠŌŅĄ“ĪŌöĒæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ŅŃÖŖ»ÆŗĻĪļA”¢B”¢C”¢D”¢E”¢F”¢GŗĶµ„ÖŹ¼×”¢ŅŅĖłŗ¬ŌŖĖŲ¾łĪŖ¶ĢÖÜĘŚŌŖĖŲ£¬AµÄÅØČÜŅŗÓė¼×ÄÜ·¢ÉśČēĶ¼ĖłŹ¾µÄ·“Ó¦£®¼×ŹĒ³£¼ūµÄŗŚÉ«¹ĢĢåµ„ÖŹ£¬ŅŅŹĒ³£¼ūµÄĘųĢåµ„ÖŹ£¬ŹĒæÕĘųµÄÖ÷ŅŖ³É·ÖÖ®Ņ»£¬BŹĒĪŽÉ«ĘųĢ壬ŹĒÖ÷ŅŖµÄ“óĘųĪŪČ¾ĪļÖ®Ņ»£¬C³£ĪĀĻĀĪŖĪŽÉ«ŅŗĢ壬EŹĒŅ»ÖÖµ»ĘÉ«µÄ¹ĢĢ壮Ēė»Ų“šĻĀĮŠĪŹĢā£®
ŅŃÖŖ»ÆŗĻĪļA”¢B”¢C”¢D”¢E”¢F”¢GŗĶµ„ÖŹ¼×”¢ŅŅĖłŗ¬ŌŖĖŲ¾łĪŖ¶ĢÖÜĘŚŌŖĖŲ£¬AµÄÅØČÜŅŗÓė¼×ÄÜ·¢ÉśČēĶ¼ĖłŹ¾µÄ·“Ó¦£®¼×ŹĒ³£¼ūµÄŗŚÉ«¹ĢĢåµ„ÖŹ£¬ŅŅŹĒ³£¼ūµÄĘųĢåµ„ÖŹ£¬ŹĒæÕĘųµÄÖ÷ŅŖ³É·ÖÖ®Ņ»£¬BŹĒĪŽÉ«ĘųĢ壬ŹĒÖ÷ŅŖµÄ“óĘųĪŪČ¾ĪļÖ®Ņ»£¬C³£ĪĀĻĀĪŖĪŽÉ«ŅŗĢ壬EŹĒŅ»ÖÖµ»ĘÉ«µÄ¹ĢĢ壮Ēė»Ų“šĻĀĮŠĪŹĢā£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 0.8 mol | B£® | 0.6 mol | C£® | 0.5 mol | D£® | 0.2 mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
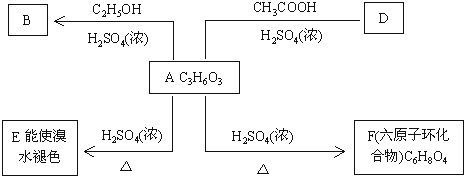

 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŌŖĖŲ±ąŗÅ ŌŖĖŲŠŌÖŹ | ¢Ł | ¢Ś | ¢Ū | ¢Ü | ¢Ż | ¢Ž | ¢ß | ¢ą |
| Ō×Ó°ė¾¶ | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| ×īøß»ņ ×īµĶ»ÆŗĻ¼Ū | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com