
����Ŀ������NaHCO3��Na2CO3��xH2O�Ļ���Ϊ�˲ⶨxֵ��ijͬѧ������ͼ��ʾ��װ�ý���ʵ��(CaCl2����ʯ�Ҿ�����)��

(1)Aװ�õ�������____________________________��
(2)Bװ�õ�������____________________________��
(3)Cװ�õ�������___________________________��
(4)����װ��A���Թ���װ��NaHCO3��Na2CO3��xH2O�Ļ����3.7 g���þƾ��Ƽ��ȵ���Ӧ��ȫ����ʱB������1.89 g��C������0.22 g����x��ֵΪ__________________��
(5)��װ�û����Ǻ����ƣ�����ʹ�ⶨ���ƫС��Ӧ��θĽ�________________��Ϊʲô��_________________________��
���𰸡�(10��)(1)������ʹNaHCO3�ֽ���ʹNa2CO3��H2Oʧˮ(1��)
(2)���շ�Ӧ�����ɵ�ˮ(1��)(3)���շ�Ӧ�����ɵ�CO2(1��)(4)10(3��)
(5)��Cװ�ú��ټ�һ��װ�м�ʯ�ҵ�U�ι�(2��)��Ϊ�˷�ֹ�����е�CO2��H2O��Cװ�õ��еļ�ʯ������(1��)
��������
���������(1)�ڼ��ȵ�������̼�������ֽ�����̼���ơ�ˮ��CO2����̼���ƾ���Ҳ��ʧȥ�ᾧˮ������Aװ�õ������Ǽ��ȣ�ʹNaHCO3�ֽ⣬ʹNa2CO3H2Oʧˮ��
(2)��ˮ�Ȼ���������ˮ������ͨ��������Ӧǰ����������Եó�ˮ���������������Bװ�õ����������շ�Ӧ�����ɵ�ˮ��
(3)���ڷ�Ӧ�л���CO2���ɣ�����ʯ�ҿ�������CO2�����ͨ��������Ӧǰ������������Եó�CO2������������Cװ�õ����������շ�Ӧ�����ɵ�CO2��
(4)�þƾ��Ƽ��ȵ���Ӧ��ȫ����ʱB������1.89g��C������0.22 g����˵����Ӧ�����ɵ�ˮ��������=1.89g��CO2����=0.22g�����ʵ����ֱ���![]() =0.105mol��
=0.105mol��![]() =0.005mol�����ݷ�Ӧ�ķ���ʽ2NaHCO3
=0.005mol�����ݷ�Ӧ�ķ���ʽ2NaHCO3![]() Na2CO3+H2O+CO2����֪���÷�Ӧ�����ɵ�CO2����0.005mol����̼�����Ƶ����ʵ�����0.005mol��2=0.01mol����Ӧ�����ɵ�ˮ��0.005mol����̼�����ڷ�Ӧ��ʧȥ��ˮ�����ʵ���=0.105mol-0.005mol=0.100mol��̼�����Ƶ�����=0.01mol��84g/mol=0.84g������Ʒ��̼���ƾ��������=3.7g-0.84g=2.86g����
Na2CO3+H2O+CO2����֪���÷�Ӧ�����ɵ�CO2����0.005mol����̼�����Ƶ����ʵ�����0.005mol��2=0.01mol����Ӧ�����ɵ�ˮ��0.005mol����̼�����ڷ�Ӧ��ʧȥ��ˮ�����ʵ���=0.105mol-0.005mol=0.100mol��̼�����Ƶ�����=0.01mol��84g/mol=0.84g������Ʒ��̼���ƾ��������=3.7g-0.84g=2.86g����![]() ��x=0.1mol�����x=10��
��x=0.1mol�����x=10��
(5)���ڿ�����Ҳ����CO2��ˮ������Ҳ�ܱ�Cװ�õ��м�ʯ�����գ��Ӷ�����C������ƫ�ߣ���˲���ֵƫ�ͣ����ԸĽ��Ĵ�ʩΪ��Cװ�ú��ټ�һ��װ�м�ʯ�ҵ�U�ιܣ�Ϊ�˷�ֹ�����е�CO2��H2O��Cװ�õ��еļ�ʯ��������


 �����ܾ�ϵ�д�
�����ܾ�ϵ�д� ���ƿ�����ϵ�д�
���ƿ�����ϵ�д� ���¿쳵����������ϵ�д�
���¿쳵����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˲ⶨһ����̬�� A �Ļ�ѧʽ��ȡһ������ A ����һ�ܱ�������ȼ �գ�����ʵ����������� CO2��CO ��ˮ������ѧ���ס����������������������Ϊ �����Լ��ķ�������� A �����ʽ�����Dz�õ���һ�������µ��й��������£�ͼ �еļ�ͷ��ʾ�����ķ���ʵ��ǰϵͳ�ڵĿ������ž�����
�ף�ȼ�ղ�����ͨ��Ũ���ᣬŨ��������2.52�ˣ���ͨ����ʯ�ң���ʯ������1.32�ˣ����ʣ��������ȼ�����ɶ�����̼1.76��
�ң�ȼ�ղ�����ͨ����ʯ�ң���ʯ������5.60�ˣ���ͨ�����ȵ�����ͭ������ͭ����0.64�ˣ����ͨ�����ȵ�����ͭ�����������ͨ�������ʯ��ˮ��ʯ��ˮ����4�ˡ�
��1���ס����������У�����Ϊ���ַ��������A�����ʽ��
��2���������ѡ��ķ�����ͨ��������� A �����ʽ����Ҫ��д��������̣�
��3����Ҫȷ��A�ķ���ʽ���Ƿ���Ҫ�ⶨ�������ݣ���˵��ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ÿ�����ʷ����仯���˷������Ӽ������������ͬ�����͵���(����)
A. �Ȼ�����������ͱ�������
B. ��ɱ���������
C. �����������ʯ�ҵ��ۻ�
D. �Ȼ��ƺ������ۻ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���SO2��˵���У�����ȷ����(����)
A. SO2������������
B. SO2���γ��������Ҫ��Ⱦ��֮һ
C. SO2��ˮ��Ӧ����H2SO4
D. ������SO2�ɱ�����������SO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������������������������
��4HCl(Ũ)+MnO2![]() MnCl2+Cl2��+2H2O
MnCl2+Cl2��+2H2O
��KClO3+6HCl=3Cl2��+KCl+3H2O
��KMnO4+HCl(Ũ)��KCl+MnCl2+Cl2��+H2O(δ��ƽ)��
��������������Ӧ���ش��й����⣺
(1)��Ӧ���������ӷ���ʽΪ________________��
(2)��Ӧ���У����������뻹ԭ�����������Ϊ____________��
(3)�뽫��Ӧ����ƽ��____KMnO4+____HCl(Ũ)=____KClʮ____MnCl2��____Cl2��+____H2O
(4)��Ҫ�Ƶ���ͬ��������������������Ӧ�е���ת�Ƶ���Ŀ֮��Ϊ___________��
(5)��֪��Ӧ����4HCl(g)+O2![]() 2Cl2+2H2O(g)���÷�ӦҲ���Ƶ���������MnO2��O2��KMnO4����������������ǿ������˳��Ϊ__________________��
2Cl2+2H2O(g)���÷�ӦҲ���Ƶ���������MnO2��O2��KMnO4����������������ǿ������˳��Ϊ__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͬѧ�ֱ�Ժ�+4����Ԫ�ص��������ʽ�����̽����
��1��������ͼװ�ý���ʵ��(�������Ѽ��������Ⱥͼг�װ������ȥ)��ʵ�����һ��ʱ���C��D�ж��������Ե���ɫ�������������ΪBaSO4��
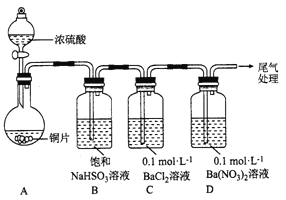
�� A�з�Ӧ�Ļ�ѧ����ʽ��______________��
��Ϊ̽��SO2��D���������ķ�Ӧ����һ��ʵ�鷢�֣�������ɫ�����Ĺ����У�D��Һ��NO3-Ũ�ȼ������䡣�ݴ˵ó����ۣ�D�г�����ɫ��������Ҫԭ����__________________��
��2����������ʵ��Ժ�+4����Ԫ�ص��������ʼ�������̽����
���� | ʵ������ | ʵ������ |
1 | ȡ0.3g����Na2SO3���壬�����м���10mL 2 mol/L������������4��BaCl2��Һ | ������ɫ����������BaCl2��Һ��ʼ������4 min����Һ����� |
2 | ȡ0.3g����Na2SO3�����������м���10mL 2 mol/L HNO3���ٵ���4��BaCl2��Һ | ������ɫ����������BaCl2��Һ������ʼ��������2 h����Һ����� |
3 | ȡ0.3g����Na2SO3���壬�����м���10mL ŨHNO3,������4��BaCl2��Һ | ��������ɫ����������BaCl2��Һ������Һ��������������ɫ���� |
�������ӷ���ʽ����ʵ��1�в��������ԭ��________________��
�� ��ʵ��1��2��3�Աȣ����Եõ�����:________________��
����ͨ���������Ϸ���.Na+��ʵ��1��2�г��ֻ��ǵ�ʱ����Ӱ�죬���ǽ�һ��̽��Cl-�� NO3-������Ӱ�죺
��� | ʵ������ | ʵ������ |
4 | ȡ____�������������м���10mL2 mol /LHNO3���ٵ���4��BaCl2��Һ | ������ɫ������������BaCl2��Һ����ʼ��������20 min����Һ����� |
i.ʵ��2��4�Աȣ��һ������:C1-�Ĵ��ڿ��Լӿ���Һ��+4����Ԫ����������
ii.ʵ��I��4�Աȣ��һ������: ______________��
��ͨ������ʵ�飬��ͬѧ��Ϊ��ȷ��ij��Һ�к���SO42-��ʵ�鷽����ȡ����Һ���������ȵμ�____________ (����ĸ���)��
a��2 mol/L���ᣬ�ٵμ�BaCl2��Һ��һ��ʱ�����ְ�ɫ����
B��2 mol/L�������ٵμ�BaCl2��Һ���������ְ�ɫ����
C��2 mol/L���ᣬ�ٵμ�BaCl2��Һ��һ��ʱ��������ɫ����
D��2 mol/L���ᣬ�ٵμ�BaCl2��Һ������������ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л���ʵ������У�����������(����)
A. ��Һ����ʱ����Һ©���¶˹ܿڼ�˴������ձ��ڱ�
B. ����ʪ��ĺ�ɫʯ����ֽ���鰱��
C. ϡ��Ũ����ʱ������ʢ��Ũ������ձ���ֱ�Ӽ�����ˮ
D. �Թܿ��þƾ���ֱ�Ӽ��ȣ�Ҳ����ˮԡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����CO2�Ʊ��״����̿����漰��Ӧ���£�
��Ӧ����CO2(g)+3H2(g) ![]() CH3OH(g) +H2O(g) ��H1=��49.58 kJmol-1
CH3OH(g) +H2O(g) ��H1=��49.58 kJmol-1
��Ӧ����CO2(g)+ H2(g) ![]() CO (g)+H2O(g) ��H2
CO (g)+H2O(g) ��H2
��Ӧ����CO(g)+2 H2(g) ![]() CH3OH(g) ��H 3=��90.77 kJmol-1
CH3OH(g) ��H 3=��90.77 kJmol-1
�ش��������⣺
��1����Ӧ������H2= ����Ӧ���Է����������� ������¡��������¡����κ��¶ȡ�����
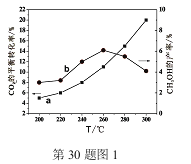
��2��ij�о�С�齫һ������H2��CO2��������ܱ������У��ں��ʵĴ��������·����˷�ӦI������������ͬ�¶�����ϵ�ﵽƽ��ʱ���CO2��ת���ʣ�a����CH3OH�IJ��ʣ�b���仯��ͼ1��ʾ��
���÷�Ӧ�ﵽƽ���Ϊ����߷�Ӧ����ͬʱ��״������������ɲ�ȡ�Ĵ�ʩ�� ��
A���ø�Ч���� B�����¶� C��С������� D������״� E����CO2��Ũ��
����ͼ1�����¶ȸ���260��ʱ��CO2��ƽ��ת�������¶ȵ����������ӣ���CH3OH�IJ���ȴ�����½�����˵������ ��
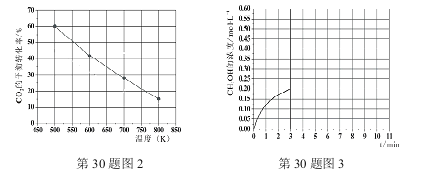
��3����֪����2L�����ܱ������г���3mol H2��1.5mol CO2��һ�������£������Ƿ�����Ӧ������ʵ�����ڲ�ͬ�¶��£���Ӧ��ϵ��CO2��ƽ��ת�������¶ȵĹ�ϵ������ͼ2��ʾ��ʵ���ã���500Kʱ����Ӧ����10minʱ�ﵽƽ�⣬���������������䣬����Ӧʱ����е�3minʱ��Ѹ�ٽ���Ӧ�¶�����600K����ʵ�飬����ͼ3�л���3��10min��������CH3OHŨ�ȵĺ����仯������ͼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1 g������ȫ�ֽ�Ϊ����������ʱ������2.72 kJ���������������Ȼ�ѧ����ʽ��ȷ������ ��
��N2��g����3H2��g��=2NH3��g�� ��H����92.4 kJ/mol
��N2��g����3H2��g��=2NH3��g�� ��H����46.2 kJ/mol
��NH3��g��=![]() N2��g����
N2��g����![]() H2��g�� ��H����46.2 kJ/mol
H2��g�� ��H����46.2 kJ/mol
��2NH3��g��=N2��g����3H2��g�� ��H����92.4 kJ/mol
A���٢� B���٢� C���٢ڢ� D��ȫ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com