
(10分)下表是A、B二种有机物的有关信息;
| A | B |
| ①能使含溴的四氯化碳溶液褪色; ②比例模型为: ③能与水在一定条件下反应 | ①由C、H两种元素组成; ②球棍模型为: |
根据表中信息回答下列问题:
(1)A与含溴的四氯化碳溶液反应的生成物的名称叫做 ;
写出在一定条件下,A生成高分子化合物的化学反应方程式__ _。
(2) A与氢气发生加成反应,其生成物的同系物的组成通式为________。
(3)B具有的性质是 (填序号):
①无色无味液体、 ②有毒、 ③不溶于水、 ④密度比水大、
⑤与酸性KMnO4溶液和溴水反应褪色、 ⑥任何条件下不与氢气反应;
写出浓硫酸和浓硝酸的混和物与B与反应的化学方程式: 。
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:阅读理解
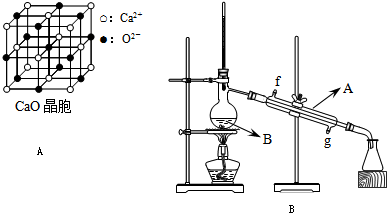
| ||
| ||


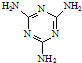 )俗称“蛋白精”.动物摄入三聚氰胺和三聚氰酸(
)俗称“蛋白精”.动物摄入三聚氰胺和三聚氰酸( 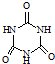 )后,三聚氰酸与三聚氰胺分子相互之间通过
)后,三聚氰酸与三聚氰胺分子相互之间通过| 化合物 | 密度/g?cm-3 | 沸点/℃ | 溶解度/100g水 |
| 正丁醇 | 0.810 | 118.0 | 9 |
| 冰醋酸 | 1.049 | 118.1 | ∞ |
| 乙酸正丁酯 | 0.882 | 126.1 | 0.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| 催化剂 |
| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |
| 催化剂 |
| 催化剂 |
| A | B |
| ①分子式为C3H8O; ②在Cu的作用下催化氧化的产物 不能发生银镜反应 |
①由C、H两种元素组成; ②球棍模型为:  |
| 浓H2SO4 |
| △ |
| 浓H2SO4 |
| △ |
 +HNO3(浓)
+HNO3(浓)| 浓H2SO4 |
| △ |

 +HNO3(浓)
+HNO3(浓)| 浓H2SO4 |
| △ |

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| 催化剂 |
| 紫外光 |
| 催化剂 |
| 紫外光 |
| 甲同学选择的试剂 | 乙同学认为不合理的理由 |
| 紫色石蕊试液 | 紫色石蕊试液B中溶液呈碱性(NaOH足量),无法证明是甲酸(酸性) 紫色石蕊试液B中溶液呈碱性(NaOH足量),无法证明是甲酸(酸性) |
| 新制氢氧化铜 | B中可能溶有过量的甲醛,无法证明是甲酸中醛基 B中可能溶有过量的甲醛,无法证明是甲酸中醛基 |
查看答案和解析>>
科目:高中化学 来源: 题型:
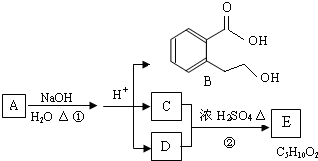
| 浓硫酸 |
| 加热 |
| 浓硫酸 |
| 加热 |


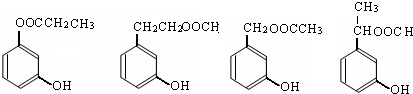 写出四者之一即可
写出四者之一即可 写出四者之一即可
写出四者之一即可| 实验编号 | C物质的量浓度(mol?L-1) | NaOH物质的量浓度(mol?L-1) | 混合溶液的pH |
| m | 0.1 | 0.1 | pH=9 |
| n | 0.2 | 0.1 | pH<7 |
查看答案和解析>>
科目:高中化学 来源:河东区一模 题型:问答题
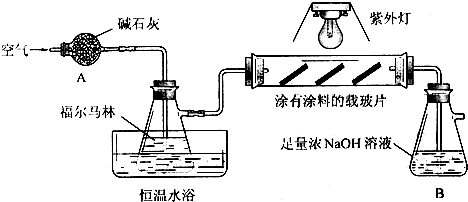
| 甲同学选择的试剂 | 乙同学认为不合理的理由 |
| 紫色石蕊试液 | ______ |
| 新制氢氧化铜 | ______ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com