H、O两种元素结合形成的化合物有H
2O和H
2O
2两种。有人提出:H
2在O
2中燃烧除生成H
2O外,是否还生成H
2O
2呢?为验证他的猜想,该学生进行如下实验:①制取氢气;②让氢气在空气中燃烧,收集所生成的液体;③将收集到的液体滴入很稀的KMnO
4溶液中,观察是否褪色。

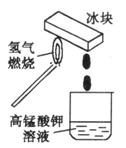
(1)采用如图所示的实验装置制取H2。如何检验该装置的气密性?
答:______________________________________________________________。
(2)实验时,在氢气燃烧的火焰上方罩上一块冰块,在火焰下方放一个装有浓度很稀的高锰酸钾溶液(如图所示)。当液滴滴入烧杯一段时间,烧杯中溶液的浅红色褪去。该现象为推,测H2O2生成提供有利证据。请配平下列反应并标明电子转移情况:
_____H2O2+______ +_______H+====_______Mn2+______H2O+______O2
+_______H+====_______Mn2+______H2O+______O2
(3)该同学后来将高锰酸钾溶液改成含有少量KSCN的FeCl2溶液(含HCl)进行实验,观察到溶液变红的现象。请写出所发生反应的化学方程式。
答:_________________________________________________。



![]() +_______H+====_______Mn2+______H2O+______O2
+_______H+====_______Mn2+______H2O+______O2![]()
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案