
��12�֣���ѧ�о���ѧϰС����ͨ��ʵ��̽�������ƵĻ�ԭ�����ۺ������ᷴӦ����FeCl2����FeCl3�����������̽�����ش��й����⣺
��1��һλͬѧ����Ӧ�����Һ�еμ�NaOH��Һ�ķ�������֤��Һ�к���Fe2+���ٿɹ۲쵽��ʵ��������___________���ڷ�Ӧ�����з�����Ӧ�Ļ�ѧ����ʽ�� ��
��2����һλͬѧ��Ӧ�����Һ���ȵμ�KSCN��Һ���������еμ�������ˮ����Һ���ֺ�ɫ�������μӹ���������ˮʱ��ȴ���ֺ�ɫ��ȥ��Ϊ��Ū����Һ��ɫ��ȥ��ԭ��ͬѧ�Dz鵽�������ϣ�
������һ�ֻ������Ϊ�����Σ�����FeO42-����
��SCN���ĵ���ʽΪ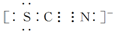
III����ˮ���к�ǿ�������ԡ�
����ͬѧ��������ּ��裺
�ٵ�һ�ּ����ǣ�Cl2�ɽ�Fe3+����ΪFeO42-����д�������ӷ�Ӧ����ʽ__________��
�ڵڶ��ּ����ǣ�____________������ü��������������___________________
��1���ٲ�����ɫ������Ѹ�ٱ�Ϊ����ɫ�����ձ�ɺ��ɫ��
��FeCl2��2NaOH===Fe��OH��2����2NaCl
4Fe��OH��2��O2��2H2O===4Fe��OH��3��
��2����2Fe3����3Cl2��8H2O===2FeO��6Cl����16H����
��SCN����Cl2�������ӵ���ʽ������SCN����SΪ�����ۣ�NΪ�����ۣ���Ϊ��ͼ��б������Ŀ���
������������Ԫ�ؼ��仯�����֪ʶ��Ϊ���������鷽��ʽ��д���������Լ�������⣬�������⣬��������������
��Fe2����2OH�D=Fe(OH)2����4Fe��OH��2��O2��2H2O===4Fe��OH��3���ٲ�����ɫ������Ѹ�ٱ�Ϊ����ɫ�����ձ�ɺ��ɫ,�ڷ���ʽ��FeCl2��2NaOH===Fe��OH��2����2NaCl��
4Fe��OH��2��O2��2H2O===4Fe��OH��3��Cl2�ɽ�Fe3+������2����2Fe3����3Cl2��8H2O===2FeO��6Cl����16H���� ��SCN����Cl2�������ӵ���ʽ������SCN����SΪ�����ۣ�NΪ�����ۣ���Ϊ��ͼ��б������Ŀ��ܡ�


 ��������ϵ�д�
��������ϵ�д� ��ӡ�Ļ���ʱ����ϵ�д�
��ӡ�Ļ���ʱ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ||
| ||

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 ��
��
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| �ζ����� ʵ������ |
1 | 2 | 3 | 4 |
| V����Ʒ��/mL | 20.00 | 20.00 | 20.00 | 20.00 |
| V ��NaOH��ʼ/mL | 0.00 | 0.20 | 0.10 | 0.10 |
| V ��NaOH����/mL | 14.98 | 15.20 | 15.12 | 16.24 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
ij��ѧ�о���ѧϰС����ⶨʳ��������(g/100mL)����������С���ʵ�鲢�ش�������⡣
��ʵ��Ŀ�ġ��ⶨʳ��������
��ʵ��ԭ�����к͵ζ�
��ʵ����Ʒ������ˮ������ʳ�ð״���Ʒ500mL(�̱�ע����������3.50g/100mL��5.00g /100mL)��
0.1000mol/LNaOH����Һ��
100mL����ƿ��10ml��Һ�ܣ���ʽ�ζ��ܣ�����̨���ζ��ܼУ���ƿ���ձ������ָʾ��(�ɹ�ѡ�õ��У����ȣ���̪��ʯ��)��
��ʵ�鲽�衿
�� ���Ʋ���ȡ����ʳ����Һ
��10mL��Һ����ȡ10mL���۰״���Ʒ����100mL����ƿ�У��ô�����������ˮϡ�����̶��ߣ�ҡ�Ⱥ�����ʽ�ζ���ȡ����ʳ����Һ20mL����������ƿ�С�
�� ʢװ��NaOH��Һ
����ʽ�ζ���ϴ������NaOH����Һ��ϴ3�Σ�Ȼ�����NaOH����Һ���ų����첿�����ݺ�ʹҺ��λ�ڡ�0���̶Ȼ�0�������¡����ã���ȡ���ݲ���¼ΪNaOH����Һ����ij�������
�� �ζ�
��ʢ�д���ʳ����Һ����ƿ�еμ�ij���ָʾ��2��3�Σ��ζ����յ㡣��¼NaOH���ն������ظ��ζ�3�Ρ�
�����ݼ�¼��
| �ζ����� ʵ������ | 1 | 2 | 3 | 4 |
| V(��Ʒ)/mL | 20.00 | 20.00 | 20.00 | 20.00 |
| V (NaOH)ʼ/mL | 0.00 | 0.20 | 0.10 | 0.10 |
| V (NaOH)��/mL | 14.98 | 15.20 | 15.12 | 16.24 |
��������˼����
�� ��������л��貹��������� �� ������ˮ�Ĵ��������� �� ��
�� ���������ѡ������ָʾ���� �� �������� �� ��
�� ������ɫʳ����ʵ�飬Ϊȷ�жϵζ��յ㣬�ɲ�ȡ�Ĵ�ʩ�� �� ��
�� ��Ʒ�������� �� g/100mL��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com