
现拟用下图所示装置(尾气处理部分略)来制取一氧化碳,并用以测定某铜粉样品(混有CuO粉末)中金属铜的含量。

(1)制备一氧化碳的化学方程式是________________________;
(2)实验中,观察到反应管中发生的现象是____________________________,尾气的主要成分是_________________________;
(3)反应完成后,正确的操作顺序为______________(填字母);
a.关闭漏斗开关;b.熄灭酒精灯1;c.熄灭酒精灯2
(4)若实验中称取铜粉样品5.0 g,充分反应后,反应管中剩余固体的质量为4.8 g,则原样品中单质铜的质量分数为__________;
(5)从浓硫酸、浓硝酸、蒸馏水、双氧水中选用合适的试剂,设计一个测定样品中金属铜质量分数的方案:
①设计方案的主要步骤是(不必描述操作过程的细节)
________________________________________________________________;
②写出有关反应的化学方程式_____________________________________。
【解析】(1)制备CO的化学方程式:HCOOH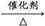 CO↑+H2O。
CO↑+H2O。
(2)实验中,观察到反应管中发生的现象是黑色粉末变红;尾气的主要成分是CO、CO2。
(3)实验步骤:先通入一会儿CO后,再加热,后停止加热,然后继续通入CO直至玻璃管冷却为止,故正确的操作顺序为先熄灭酒精灯2,然后关闭漏斗开关,最后熄灭酒精灯1。
(4)若实验中称取铜粉样品5.0 g,充分反应后,反应管中剩余固体的质量为4.8 g,剩余固体全部为铜,由差量法
CuO+CO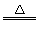 Cu+CO2 Δm
Cu+CO2 Δm
80 g 64 g 16 g
m(CuO) (5.0-4.8)g=0.2 g
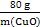 =
=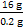 m(CuO)=1.0 g
m(CuO)=1.0 g
m(Cu)=m(样品)-m(CuO)=4.0 g m(样品)=5.0 g
原样品中单质铜的质量分数为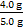 ×100%=80%。
×100%=80%。
(5)要测定铜的质量分数,需要把浓硫酸稀释,氧化铜和稀硫酸反应,铜和稀硫酸不反应,即可求出铜的质量分数。设计实验方案的主要步骤:将浓硫酸用蒸馏水稀释,让样品与稀硫酸充分反应后,过滤,干燥,称量剩余固体铜的质量。反应的化学方程式为CuO+H2SO4====CuSO4+H2O。
答案:(1)HCOOH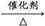 CO↑+H2O
CO↑+H2O
(2)样品粉末逐渐变红色 CO、CO2
(3)c、a、b
(4)80%
(5)①将浓硫酸用蒸馏水稀释,让样品与稀硫酸充分反应后,过滤、洗涤、干燥、称重、计算
②CuO+H2SO4====CuSO4+H2O


科目:高中化学 来源: 题型:
已知某人每日所需热量为12 000 kJ,每克糖类、蛋白质、油脂在人体内氧化所提供的热量分别为16.7 kJ、16.7 kJ、37.7 kJ;又已知糖类、蛋白质、油脂对人体内所需热能所占的百分数分别为60%~70%、10%~15%、20%~25%。试判断该人每日摄入500 g淀粉、100 g蛋白质、65 g油脂是否合乎平衡膳食的要求。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.在离子晶体中,一定存在离子键
B.阳离子只有氧化性,阴离子只有还原性
C.纳米粒子分散到水中,有丁达尔现象
D.等离子体是由大量的带电微粒组成的,是继固体、液体、气体之后物质的另一种聚集状态
查看答案和解析>>
科目:高中化学 来源: 题型:
往两支分别装有浅绿色的Fe(NO3)2和FeSO4溶液的试管中分别逐滴加入稀盐酸时,溶液的颜色变化应该是( )
A.前者基本没有改变,后者变棕黄色
B.前者变棕黄色,后者也变棕黄色
C.前者变棕黄色,后者基本没有改变
D.前者、后者都基本没有改变
查看答案和解析>>
科目:高中化学 来源: 题型:
某课外活动小组在学习CO的化学性质时,准备做CO还原CuO的实验。下面是同学们设计的四套实验装置图。从安全和能源充分利用的角度来看,你认为最理想的实验装置是( )
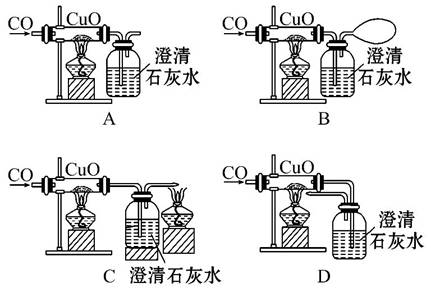
查看答案和解析>>
科目:高中化学 来源: 题型:
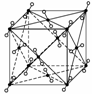
干冰晶体是一种面心立方结构,如图所示,即8个CO2分子构成立方体的8个顶点,6个面的中心又各有1个CO2分子,在每个CO2分子周围与它的距离为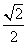 a(其中a为立方体棱长)的CO2分子有( )
a(其中a为立方体棱长)的CO2分子有( )
A.4个 B.8个
C.12个 D.6个
查看答案和解析>>
科目:高中化学 来源: 题型:
分子晶体在通常情况下不具有的性质是( )
A.晶体构成微粒是分子
B.干燥或熔化时均能导电
C.微粒间以范德华力结合
D.熔点、沸点一般低于原子晶体和离子晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B为两种短周期元素,A的原子序数大于B,且B原子的最外层电子数为A原
子最外层电子数的3倍。A、B形成的化合物是中学化学常见的化合物,该化合物熔融
时能导电。试回答下列问题:
(1)A、B的元素符号分别是________、________。
(2)用电子式表示A、B元素形成化合物的过程:_____________________________
________________________________________________________________________。
(3)A、B所形成的化合物的晶体结构与氯化钠晶体结构相似,则每个阳离子周围吸引了
________个阴离子;晶体中阴、阳离子数之比为__________。
(4)A、B所形成化合物的晶体的熔点比NaF晶体的熔点________,其判断的理由是
________________________________________________________________________________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com