
【题目】某同学向100mL NH4Al(SO4)2溶液中加入0.1 mol·L-1NaOH溶液,产生沉淀的图像如下:
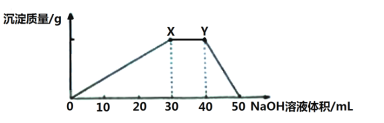
下列说法不正确的是
A.NH4Al(SO4)2溶液中含0.003 mol Al3+
B.NH4Al(SO4)2溶液中NH4+的浓度是0.01 mol·L-1
C.Al3+结合OH-的能力比NH4+强
D.Y点之后发生反应的离子方程式是:Al(OH)3+ OH-= AlO2-+2H2O
【答案】A
【解析】
向100mL 0.1 mol·L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1 mol·L-1 NaOH溶液,首先生成氢氧化铝沉淀。当铝离子恰好沉淀完后,此时对应X点;继续加入氢氧化钠,铵根开始转化为一水合氨,铵根恰好完全转化为一水合氨,此时对应Y点。继续加入氢氧化钡,则氢氧化铝开始溶解,最终完全溶解。
A. Y点之后氢氧化铝开始溶解,共消耗0.01L×0.1 mol·L-1=0.001molNaOH,根据反应Al(OH)3 + NaOH = NaAlO2 + 2H2O可知,n(Al(OH)3)=n(NaOH)=0.001mol,故A错误;
B. X点后继续加入氢氧化钠,铵根开始转化为一水合氨,铵根恰好完全转化为一水合氨,此时对应Y点,共消耗0.01L×0.1 mol·L-1=0.001molNaOH,根据反应NH4++OH-=NH3H2O可知,n(NH4+)=n(NaOH)=0.001mol,故B正确;
C. Al3+先和氢氧根反应生成沉淀,则Al3+结合OH-的能力比NH4+强,故C正确;
D. Y点后继续加入氢氧化钡,则氢氧化铝开始溶解,最终完全溶解,离子方程式为:Al(OH)3+ OH-= AlO2-+2H2O,故D正确;
题目要求选择不正确的,故选A。


科目:高中化学 来源: 题型:
【题目】已知:2C(s)+O2(g)===2CO(g) ΔH=-Q1kJ·mol-1;
C(s)+O2(g)===CO2(g) ΔH=-Q2kJ·mol-1;
S(s)+O2(g)===SO2(g) ΔH=-Q3kJ·mol-1。
CO与镍反应会造成镍催化剂中毒,为防止镍催化剂中毒,工业上常用SO2将CO氧化,二氧化硫转化为单质硫,则该反应的热化学方程式为 ( )
A. SO2(g)+2CO(g)===S(s)+2CO2(g) ΔH=(2Q1-2Q2+Q3) kJ·mol-1
B. S(s)+2CO(g)===SO2(g)+2C(s) ΔH=(Q1-Q3) kJ·mol-1
C. SO2(g)+2CO(g)===S(s)+2CO2(g) ΔH=(Q1-2Q2+Q3) kJ·mol-1
D. SO2(g)+2CO(g)===S(s)+2CO2(g) ΔH=(2Q1-Q2+2Q3) kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏伽德罗常数的值,下列叙述正确的是
A.0.1mol Fe与100mL 1mol·L-1盐酸充分反应,溶液中的Fe2+数目为0.1NA
B.0.1mol·L-1(NH4)2SO4溶液中含SO42-数目为0.1NA
C.常温常压下,1.8g H2O中含有的分子数为0.1NA
D.33.6LNO2和足量水反应转移的电子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,甲、乙、丙分别表示在不同条件下,可逆反应A(g)+B(g)![]() xC(g)的生成物C的百分含量w(C)和反应时间(t)的关系。
xC(g)的生成物C的百分含量w(C)和反应时间(t)的关系。
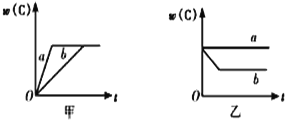
(1)若甲中两条曲线分别代表有催化剂和无催化剂的情况,则_____曲线代表无催化剂时的情况。
(2)若乙表示反应达到平衡状态后,分别在恒温恒压条件下和恒温恒容条件下向平衡混合气体中充入He后的情况,则____曲线表示恒温恒容的情况,且此时混合气体中w(C)____(填“变大”“变小”或“不变”)。
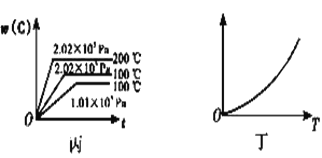
(3)根据丙可以判断该可逆反应的正反应是____(填“放热”或“吸热”)反应,x的值为____。
(4)丁表示在某固定容积的密闭容器中,上述可逆反应达到平衡后,某物理量随温度(T)的变化情况,根据你的理解,丁的纵坐标可以是_____ (填序号)。
①w(C) ②A的转化率 ③压强 ④c(B)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定质量的某铁的氧化物FexOy与100mL 0.1 mol·L-1 稀硫酸恰好反应完全,得到溶液Z。若用相同质量的该铁的氧化物与CO或H2在高温下反应,反应需要标准状况下CO或H2的体积分别为V1和V2。下列说法正确的是
A.x=2、y=3B.Z溶液一定能使酸性KMnO4溶液褪色
C.V1=V2D.V1和V2的体积不能确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将铁粉和铝粉的混合物逐渐加入100mL的稀硝酸中,其产生的有关离子浓度与加入铁粉和铝粉的混合物的质量的关系如下图所示:
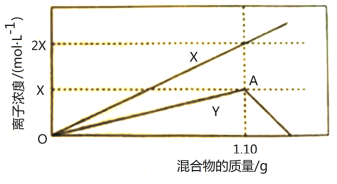
若反应过程中生成的气体为NO,溶液的体积变化忽略不计。请回答下列问题:
(1)X表示的变化离子是_______________(填离子符号)。
(2)OA段发生反应的离子方程式是___________________________________。
(3)稀硝酸溶解1.10g铁粉和铝粉后溶液还能继续溶解混合物的原因是________________
(4)该硝酸的浓度是_____________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二酸(H2C2O4)俗称草酸,在实验研究和化学工业中应用广泛。草酸溶液中各粒子的物质的量分数随溶液pH变化关系如下图,下列说法正确的是
已知:①室温下,0.1 mol· L-1 H2C2O4的pH=1.3 ;0.1 mol· L-1NaHC2O4的pH=2.8
②草酸钙(Ca C2O4)难溶于水;
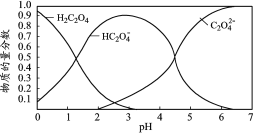
A.pH=4.5的草酸溶液中含有的大量微粒有:H2C2O4、HC2O4-、C2O42-
B.0.1 mol·L1 NaHC2O4溶液中:c(Na+)>c(HC2O4-)>c(C2O42-)>c(H2C2O4)
C.向H2C2O4溶液中加入酸性高锰酸钾溶液,紫色褪去:2MnO4-+5C2O42-+16H+=2Mn2+ +10CO2↑ +8H2O
D.向NaHC2O4溶液中加入足量澄清石灰水,产生白色沉淀:2HC2O4- +Ca2++2OH-=Ca C2O4↓ +2H2O+C2O42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子团SCN化合价为-1价,在很多方面跟卤素原子相似,因此称为“拟卤素”。拟卤素离子与卤离子还原性强弱顺序为Cl-<Br-<SCN-<I-,又知氧化性I2>S,下列反应不正确的是( )
A. (SCN)2+2Br-=Br2+2SCN-
B. (SCN)2+H2S=2H++2SCN-+S↓
C. 4H++2SCN-+MnO2![]() Mn2++(SCN)2↑+2H2O
Mn2++(SCN)2↑+2H2O
D. (SCN)2+2I-=2SCN-+I2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com