
| A. | N2H4(g)+2H2O2(l)=N2(g)+4H2O(l)△H=+817.63 kJ•mol-1 | |
| B. | N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)△H=-641.63 kJ•mol-1 | |
| C. | N2H4(g)+2H2O2(l)=N2(g)+4H2O(l)△H=-641.63 kJ•mol-1 | |
| D. | N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)△H=-817.63 kJ•mol-1 |
分析 根据已知热化学方程式和目标反应的热化学反应方程式,利用盖斯定律来解答.
解答 解:N2H4(g)+O2(g)=N2(g)+2H2O(g)△H1=-533.23kJ•mol-1 ①
H2O(g)=H2O (l)△H2=-44kJ•mol-1 ②
2H2O2(l)=2H2O(l)+O2(g)△H3=-196.4kJ•mol-1 ③
则联氨与过氧化氢反应的热化学方程式可用①+②×2+③:N2H4(g)+2H2O2(l)=N2(g)+4H2O(l)△H=-817.63kJ•mol-1
或用①-②×2+③:N2H4(g)+2H2O2(l)=N2(g)+4H2O(l)△H=-641.63kJ•mol-1,
故选C.
点评 本题考查了热化学方程式的书写与盖斯定律的应用,题目难度不大,把握盖斯定律的原理和热化学方程式的书写规则为解题的关键.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
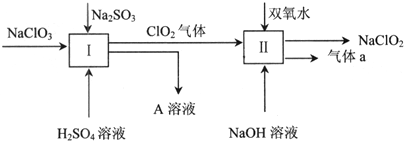
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 原子序数依次增加的X、Y、Z、W四种元素原子序数均小于36,Y基态原子最外层电子数是其内层电子总数的3倍,X、W基态原子是同周期元素中未成对电子数最多的原子,X与Z的原子核内质子数之和等于W原子核内质子数,Z基态原子只有1个未成对的电子.
原子序数依次增加的X、Y、Z、W四种元素原子序数均小于36,Y基态原子最外层电子数是其内层电子总数的3倍,X、W基态原子是同周期元素中未成对电子数最多的原子,X与Z的原子核内质子数之和等于W原子核内质子数,Z基态原子只有1个未成对的电子. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 取ag混合物充分加热,剩余bg固体 | |
| B. | 取ag混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重bg | |
| C. | 取ag混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得bg固体 | |
| D. | 取ag混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得bg固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | P的平均反应速率是0.15mol/(L•min) | B. | Q的转化率是25% | ||
| C. | Q的平衡浓度是1mol/L | D. | x的值为2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
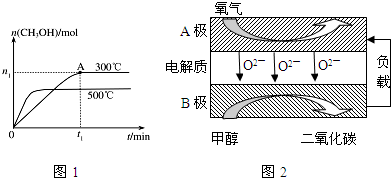
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3:2:2:4 | B. | 1:1:1:1 | C. | 2:1:1:2 | D. | 1:2:1:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com