

分析 (1)测量白色固体中碳酸钠的质量分数:①按图连接好装置;④检查装置的气密性;②用托盘天平准确称取该样品2.0g,放入B中试管内,向C中集气瓶中倒入水至瓶颈处,然后倒入少许植物油;③向B中试管内加入稀硫酸至过量;读取A中液体体积得到生成二氧化碳的气体;
(2)样品中通过分液漏斗加入稀硫酸反应生成二氧化碳气体通过装置C和A组成排水量气法测定生成的二氧化碳气体的体积;
(3)植物油防止二氧化碳溶解;
(4)反应结束后,量筒中收集到水220mL,该状况下二氧化碳的密度为2.0g/L,计算得到二氧化碳质量=0.220L×2.0g/L=0.44g,元素守恒得到碳酸钠物质的量,质量分数=$\frac{物质质量}{样品质量}$×100%;
(5)读取量筒内液体体积时仰视读数读取体积减小.
解答 解:(1)测量白色固体中碳酸钠的质量分数:①按图连接好装置;④检查装置的气密性;②用托盘天平准确称取该样品2.0g,放入B中试管内,向C中集气瓶中倒入水至瓶颈处,然后倒入少许植物油;③向B中试管内加入稀硫酸至过量;读取A中液体体积得到生成二氧化碳的气体,上述实验步骤正确的操作顺序为①④②③,
故答案为:①④②③;
(2)装置B中的样品中通过分液漏斗加入稀硫酸反应生成二氧化碳气体,通过装置C和A组成排水量气法测定生成的二氧化碳气体的体积,装置导管口正确的连接顺序为bdca,
故答案为:bdca;
(3)C装置中植物油的作用是,避免二氧化碳溶解在水里而损耗,造成测定结果偏低,
故答案为:避免二氧化碳溶解在水里而损耗,造成测定结果偏低;
(4)反应结束后,量筒中收集到水220mL,该状况下二氧化碳的密度为2.0g/L,计算得到二氧化碳质量=0.220L×2.0g/L=0.44g,n(CO2)=n(Na2CO3)=$\frac{0.44g}{44g/mol}$=0.01mol,碳酸钠质量分数=$\frac{物质质量}{样品质量}$×100%=$\frac{0.01mol×106g/mol}{2.0g}$×100%=50.3%,
故答案为:50.3%;
(5)在读取量筒内液体体积时仰视读数,读取量筒内液体体积时仰视读数读取体积减小,测定的结果将偏低,
故答案为:偏低.
点评 本题考查了物质组成和成分的实验探究、实验过程的理解应用、注意装置的连接,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 乙醇和乙二醇互为同系物 | |
| B. | 异丙苯( )分子中碳原子可能都处于同一平面 )分子中碳原子可能都处于同一平面 | |
| C. | 按系统命名法,化合物( )的名称是2,3,5,5一四甲基一4,4一二乙基己烷 )的名称是2,3,5,5一四甲基一4,4一二乙基己烷 | |
| D. |  的一溴代物和 的一溴代物和 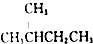 的一溴代物都有4种(不考虑立体异构) 的一溴代物都有4种(不考虑立体异构) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在常温常压下,11.2L Cl2含有的分子数为0.5NA | |
| B. | 在常温常压下,25.5g NH3所含的原子数为6NA | |
| C. | 标准状况下,11.2L水所含的分子数为0.5NA | |
| D. | 在同温同压下,相同体积的任何气体单质所含的原子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 如图是甲、乙两种固体物质的溶解度曲线.据图回答:
如图是甲、乙两种固体物质的溶解度曲线.据图回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100 mL 1 mol/L的盐酸中含HCl分子数为0.1NA | |
| B. | 7.8 g Na2O2和Na2S的混合物中阴离子数目为0.2NA | |
| C. | 标准状况下,2.24 L SO3中含有氧原子数目为0.3NA | |
| D. | 2 g D216O中含中子、质子、电子数目均为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锅炉水垢用Na2CO3溶液浸泡一段时间后,可用盐酸溶解 | |
| B. | 向Mg(OH)2悬浊液中滴加FeCl3溶液,固体颜色变深 | |
| C. | NaH2PO4溶液显酸性,Na2HPO4溶液显碱性,两种溶液中都有电离平衡和水解平衡 | |
| D. | 等物质的量浓度的(NH4)2CO3,(NH4)2SO4,(NH4)2Fe(SO4)2三种溶液,NH${\;}_{4}^{+}$浓度相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池示意图如右,该燃料电池工作时,外电路中电子的流动方向是从电极1到电极2;电池的总反应为4NH3+3O2=2N2+6H2O.
瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池示意图如右,该燃料电池工作时,外电路中电子的流动方向是从电极1到电极2;电池的总反应为4NH3+3O2=2N2+6H2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com