
| A. | 硫酸 | B. | 硝酸 | C. | 玻璃 | D. | 铝 |
分析 发生的反应中元素的化合价变化,则发生氧化还原反应,反之不发生氧化还原反应,以此来解答.
解答 解:A.利用硫铁矿高温煅烧生成二氧化硫,再发生催化氧化生成三氧化硫,S元素的化合价升高,发生氧化还原反应,故A不选;
B.合成氨后氧化生成NO,NO氧化生成二氧化氮,N元素的化合价变化,发生氧化还原反应,故B不选;
C.发生碳酸钙与二氧化硅反应等,玻璃工业的反应类型主要是复分解反应,不涉及氧化还原反应,故C选;
D.氧化铝电解生成Al,Al元素的化合价变化,为氧化还原反应,故D不选;
故选C.
点评 本题考查氧化还原反应,为高频考点,本题注意把握常见工业生产原理为解答的关键,注重基础知识的积累,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 最高正价由低到高的顺序为:X、Z、Y、W | |
| B. | 原子半径由小到大的顺序为:X、Y、Z、W | |
| C. | 最外层电子数由少到多的顺序为:X、Z、Y、W | |
| D. | 简单氢化物的稳定性由弱到强的顺序为:Y、Z、W |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=6的纯水中,c(OH-)=10-8 mol•L-1 | |
| B. | 向0.1 mol•L-1Na2SO3溶液中加入少量NaOH固体,c(Na+)、c(SO32-)均增大 | |
| C. | 室温下,pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合后溶液pH>7 | |
| D. | 0.1 mol•L-1Na2CO3溶液中c(OH-)=c(H+)+c(HCO3-)+c(H2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
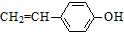 )常用于肉香和海鲜香精配方中.
)常用于肉香和海鲜香精配方中.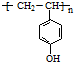 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | 方法 | 试剂 | |
| A | CO2(SO2) | 洗气 | 氢氧化钠溶液 |
| B | 氯化亚铁溶液(氯化铁) | 过滤 | 铁粉 |
| C | 水(溴) | 萃取、分液 | 酒精 |
| D | 硫酸钠(氯化铵) | 加热 | 氢氧化钠 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 2:1 | C. | 3:1 | D. | 4:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用活性炭除去冰箱中的异味是发生了化学反应 | |
| B. | 碘是人体必需微量元素,所以要多吃富含碘化钾的食物 | |
| C. | 可以利用氯化铁溶液的酸性清除铜镜表面的铜锈 | |
| D. | 航天服主要成分是由碳化硅、陶瓷和碳纤维复合而成,它是一种新型无机非金属材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com