
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
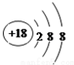
分析 由元素在周期表中位置,可知①为N、②为F、③为Na、④为Mg、⑤为Al、⑥为Si、⑦为Cl、⑧为Ar、⑨为K、⑩为Br,
(1)稀有气体Ar的性质最稳定;
(2)这些元素的最高价氧化物对应的水化物中,高氯酸的酸性最强,KOH的碱性最强,氢氧化铝具有两性;
(3)⑤的最高价氧化物对应水化物为氢氧化铝,与氢氧化钠溶液反应生成偏铝酸钠和水;
(4)先根据HXR气体的质量和体积求出其摩尔质量,然后根据相对分子质量和R在该氢化物中的质量分数求出R的原子量,得出元素R是何种元素,即可得到化学式,以此来解答.
解答 解:由元素在周期表中位置,可知①为N、②为F、③为Na、④为Mg、⑤为Al、⑥为Si、⑦为Cl、⑧为Ar、⑨为K、⑩为Br,
(1)稀有气体Ar的性质最稳定,其原子结构示意图为 ,故答案为:
,故答案为: ;
;
(2)这些元素的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3,
故答案为:HClO4;KOH;Al(OH)3;
(3)⑤的最高价氧化物对应水化物为氢氧化铝,与氢氧化钠溶液反应生成偏铝酸钠和水,离子反应方程式为Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(4)8.5g的HXR气体在标准状态下的体积是5.6L,
n=$\frac{5.6L}{22.4L/mol}$=0.25mol,
M=$\frac{8,5g}{0.25mol}$=34g/mol,所以HXR的相对分子量为34;
R在该氢化物中的质量分数为94%,则$\frac{R}{34}$×100%=94%,解得R=32,即R为S,所以HXR的化学式为H2S,
故答案为:34;H2S.
点评 本题考查位置、结构与性质的应用,为高频考点,把握元素的位置推断元素为解答的关键,侧重分析与推断能力的考查,注意元素周期律及元素化合物知识的应用,题目难度不大.


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:解答题
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | R为ⅤA族元素 | |
| B. | R的氢化物的水溶液属于强酸 | |
| C. | 氧化剂与还原剂的物质的量之比为5:1 | |
| D. | R2在常温常压下一定是气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 族 周期 | I A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | J | F | H |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


 .
. .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KNO3 | B. | NaCl | C. | Na2CO3 | D. | FeSO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com