
非诺洛芬是一种治疗类风湿性关节炎的药物,可通过以下方法合成:
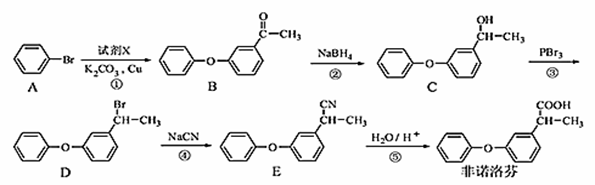
请回答下列问题:
(1)非诺洛芬中的含氧官能团为 和 (填名称)。
(2)化合物A的分子式为 。
(3)反应④的反应类型是 。
(4)化合物D与NaOH醇溶液反应的方程式 。
(5)B的一种同分异构体满足下列条件:
Ⅰ.能发生银镜反应,其水解产物之一能与FeCl3溶液发生显色反应。
Ⅱ.分子中含有两个苯环,且分子中有6种不同化学环境的氢。
写出该同分异构体的结构简式: 。
(6)利用类似上述非诺洛芬的合成方法,写出以 为原料制备
为原料制备 的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
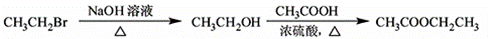
【答案】(1)醚键;羧基(2)C6H5Br(3)取代反应
(4)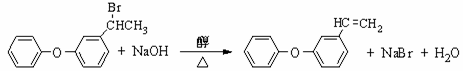
(5)
(6)

【解析】本题考查了有机物的合成。根据流程图中,A发生取代反应生成B,B发生还原反应生成C,C发生取代反应生成D,D发生取代反应生成E,E发生水解反应生成非诺洛芬。
(1)该物质中的官能团是醚键和羧基。
(2)由A的结构简式可知A的分子式为C6H5Br。
(4)由D和E的结构简式可知,反应④为取代反应。
(4)由D的结构简式可知,D中含有官能团-Br,且含溴原子的碳的相邻碳上有氢原子,则D与NaOH醇溶液可发生消去反应,反应的方程式为
 。
。
(5)Ⅰ、能发生银镜反应,说明含有醛基,其水解产物之一能与FeCl3溶液发生显色反应,说明含有酚羟基;
Ⅱ、分子中有6种不同化学环境的氢,且分子中含有两个苯环,说明该分子中含有两个苯环且H原子种类是6,则符合条件的结构简式为
 。
。
(6)由非诺洛芬的合成方法可知, 与PBr3反应可生成
与PBr3反应可生成 ,
, 与NaCN反应可生成
与NaCN反应可生成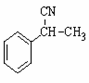 ,
, 在H2O/H+条件下可生成
在H2O/H+条件下可生成 ,故其合成路线图为:
,故其合成路线图为:
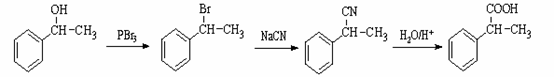


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
未来新能源的特点是资源丰富,在使用时对环境无污染或者污染很小,且可以再生.下列能源符合未来新能源标准的是( )
①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能.
|
| A. | ①②③④ | B. | ⑤⑥⑦⑧ | C. | ③⑤⑥⑦⑧ | D. | ③④⑤⑥⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关金属腐蚀与防护的说法正确的是( )
|
| A. | 纯银器表面在空气中因电化学腐蚀渐渐变暗 |
|
| B. | 当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用 |
|
| C. | 在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
|
| D. | 可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
从某废触媒[主要成分为活性炭、ZnO、FeO、(CH3COO)2Zn]中制取醋酸锌晶体的实验步骤如图:
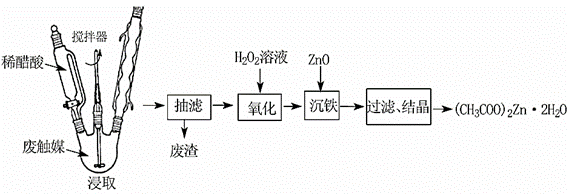
(1)浸取时,在三口烧瓶中加入废触媒及稀醋酸,给三口烧瓶加热并同时开动搅拌器的目的是 。
(2)若先将废触媒在马弗炉中通氧气500℃处理一段时间,浸出率会大大提高,其原因是 。抽滤时用的硅酸盐质仪器有 和 。
(3)流程图中加入H2O2的目的是 。
(4)所得晶体(CH3COO)2Zn·2H2O热重分析(TG/%=固体样品的剩余质量/固体样品的起始质量),文献表明分解分三个阶段,在200℃以下脱去两分子结晶水,形成的(CH3COO)2Zn在242℃熔融,370℃完全分解为ZnO同时生成CO2及一种含氧衍生物(核磁共振氢谱只有1组峰)。(CH3COO)2Zn分解生成氧化锌的反应方程式为 。

查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关反应的离子方程式的书写中,正确的是
A.C12通入水中:C12+H2O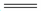 2H++Cl-+ClO-
2H++Cl-+ClO-
B.硫酸铝溶液与过量氨水反应:Al3++3NH3·H2O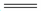 3
3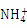 +Al(OH)3↓
+Al(OH)3↓
C.实验室用石灰石和盐酸反应制取
D.向Na2SO3溶液中加入稀硝酸:
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的性质与应用对应关系正确的是
A.FeCl3溶液显酸性,可用于蚀刻印刷电路板
B.Na2CO3溶液显碱性,可用于除锅垢中的硫酸钙
C.MgO、Al2O3熔点高,可用于制作耐高温坩埚
D.Na、K合金具有强还原性,可用于原子反应堆的导热剂
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学分析Zn与稀H2SO4的反应。
(1)该反应的离子方程式是 。
(2)制H2时,用稀硫酸而不用浓硫酸,原因是_________。
(3)已知:Zn(s)+1/2O2(g)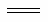 ZnO(s) ΔH=-332 kJ/mol
ZnO(s) ΔH=-332 kJ/mol
ZnO(s) + H2SO4(aq) 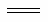 ZnSO4(aq) + H2O(l) ΔH =-112kJ/mol
ZnSO4(aq) + H2O(l) ΔH =-112kJ/mol
H2(g) +1/2 O2(g)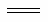 H2O(l) ΔH =-286kJ/mol
H2O(l) ΔH =-286kJ/mol
则Zn与稀H2SO4反应生成1mol H2 时的反应热ΔH = kJ/mol。
(4)该同学用如下装置进行实验,分析影响反应速率的因素。

实验时,从断开K开始,每间隔1分钟,交替断开或闭合K,并连续计数每1 分钟内从a管流出的水滴数,得到的水滴数如下表所示:
| 1分钟水滴数(断开K) | 34 | 59 | 86 | 117 | … | 102 |
| 1分钟水滴数(闭合K) | 58 | 81 | 112 | 139 | … | 78 |
分析反应过程中的水滴数,请回答:
①由水滴数58>34、81>59,说明在反应初期,闭合K时比断开K时的反应速率______(填“快”或“慢”),主要原因是_________。
②由水滴数102>78,说明在反应后期,断开K时的反应速率快于闭合K时的反应速率,主要原因是_________。
③ 从能量转换形式不同的角度,分析水滴数86>81、117>112的主要原因是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定量的盐酸跟过量的铁粉反应时,为了减缓反应速度,且不影响生成氢气的总量,可向盐酸中加入适量的( )
①NaOH固体 ②H2O ③NH4Cl固体 ④CH3COONa固体 ⑤NaNO3固体 ⑥KCl溶液.
|
| A. | ②④⑥ | B. | ①② | C. | ②③⑤ | D. | ②④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取.纯净的A为无色粘稠液体,易溶于水.为研究A的组成与结构,进行了如下实验:
| 实 验 步 骤 | 解 释 或 实 验 结 论 |
| (1)称取A 9.0g,升温使其汽化,测其密度是相同条件下H2的45倍. | 试通过计算填空: (1)A的相对分子质量为: . |
| (2)将此9.0gA在足量纯O2充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4g和13.2g. | (2)A的分子式为: C3H6O3 . |
| (3)另取A 9.0g,跟足量的NaHCO3粉末反应,生成2.24LCO2(标准状况),若与足量金属钠反应则生成2.24LH2(标准状况). | (3)用结构简式表示A中含有的官能团: . |
| (4)A的核磁共振氢谱如下图:
| (4)A中含有 种氢原子. |
| (5)综上所述,A的结构简式 , 若有手性碳原子,请在结构简式上用*标出手性碳原子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com