
| A. | 75%的酒精溶液 | B. | 硝酸钠 | C. | 碱石灰 | D. | 豆浆 | ||||
| E. | 过氧化钠 |
分析 混合物是两种或两种以上的物质组成,纯净物是单一的一种物质,由同种分子构成的物质是纯净物,由不同种分子构成的物质是混合物.
解答 解:混合物是两种或两种以上的物质组成,纯净物是单一的一种物质,由同种分子构成的物质是纯净物,由不同种分子构成的物质是混合物.
Ba(OH)2(固体)、CuSO4(固体)、纯醋酸(液态)都只含有一种物质,是纯净物.
A.75%的酒精溶液是乙醇和水的混合物,故A错误;
B、硝酸钠是纯净物,故B正确;
C.碱石灰是混合物,故C错误;
D.豆浆是蛋白质,水等的混合物,故D错误;
E.过氧化钠是纯净物,故E正确;
故选BE.
点评 本题考查混合物纯净物的概念,注意对概念的理解和区分,正确从宏观组成和微观构成两个角度来把握,还要注意特殊情况,比如碳单质和金属单质及稀有气体都是又原子直接构成的,题目较简单.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:Na>Si>Cl | B. | 还原性:Na>Mg>Al | ||
| C. | 稳定性:SiH4>H2S>HCl | D. | 酸性:H3PO4<H2SO4<HClO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
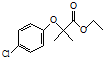 )是临床上一种降脂抗血栓药物,它的一条合成路线如下:
)是临床上一种降脂抗血栓药物,它的一条合成路线如下: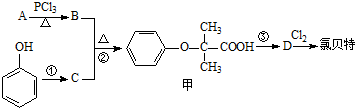
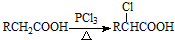
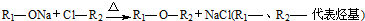
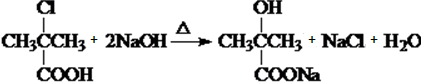 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 现象解释(用离子方程式表示) | |
| 探究① | (3)用玻璃棒蘸取Na2S2O3溶液点在pH试纸中部,将试纸颜色与标准比色卡对照 | 溶液PH=8 | (4)S2O32-+H2O?HS2O3-+OH- |
| 探究② | 向新制氯水(PH<2)中滴加少量Na2S2O3溶液 | 氯水颜色变浅 | (5)Na2S2O3具有还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
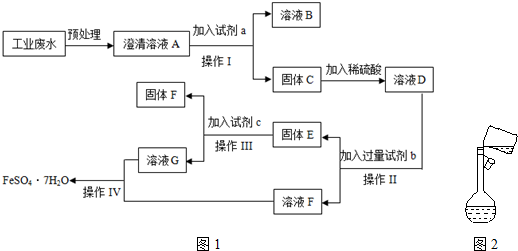
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na在常温下,与空气中的氧气不反应,所以Na不活泼 | |
| B. | Na在空气中燃烧,发出黄色火焰,产物是Na2O | |
| C. | Na是银白色金属,硬度大、熔点高 | |
| D. | Na应保存在煤油中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X有两种常见氧化物,所含的化学键类型完全相同 | |
| B. | N与M形成的化合物的水溶液显酸性 | |
| C. | 离子半径:N>X,Y>M | |
| D. | 气态氢化物的稳定性:Y>M |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com