

| A、可用A装置除去氯气中的氯化氢气体 |
| B、可用B装置量取16.20mL的NaOH溶液 |
| C、可用C实验证明氧化性:Cl2>Br2>S |
| D、可用D装置证明非金属性:S>C>Si |


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:
| A、Na+、K+、OH-、Cl- |
| B、Na+、Cu2+、SO42-、NO3- |
| C、Mg2+、Na+、SO42-、Cl- |
| D、Ba2+、Cl-、NO3-、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、纯重水中pD=7 |
| B、1L溶有0.01molNaOD的D2O溶液中,溶液的pD=12 |
| C、1L溶有0.01molDCl的D2O溶液中,溶液的pD=2 |
| D、在100mL0.25mol/LNaOD的重水中,加入50mL0.2mol/L的DCl的重水溶液,其pD=1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、恒容时,通入x气体,y的物质的量浓度增大 |
| B、恒容时,通入x气体,反应器中温度升高 |
| C、恒容时,通入惰性气体,各反应速率不变 |
| D、恒压时,通入惰性气体,c的物质的量不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③⑤⑥ | B、①②④⑤ |
| C、①②③④ | D、只有①③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素非金属性Cl>S的实验依据是酸性HClO4>H2SO3 |
| B、碳元素的电负性小于氧元素,每个CO2分子中有4个σ键 |
| C、同周期主族元素的原子形成的简单离子的电子层结构一定相同 |
| D、Na、Mg、Al三种元素,其第一电离能由大到小的顺序为Mg>Al>Na |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2、I2、HI 平衡混合气体加压后颜色变 |
| B、配制FeSO4溶液时在溶液中加入稀硫酸 |
| C、合成氨工业采用高温条件 |
| D、工业制硫酸中,SO2氧化成SO3,往往需使用催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、比列模型 可以表示二氧化硫分子,也可以表示二氧化碳分子 可以表示二氧化硫分子,也可以表示二氧化碳分子 |
B、电子式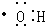 可以表示羟基,也可以表示氢氧根离子 可以表示羟基,也可以表示氢氧根离子 |
C、离子结构示意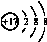 可以表示36Cl-,也可以表示37Cl- 可以表示36Cl-,也可以表示37Cl- |
| D、D结构简式(CH3)2CHOH可以表示1-丙醇,也可以表示2-丙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯中的甲苯(酸化高锰酸钾溶液 分液) |
| B、乙醇中的水(无水硫酸铜 干燥) |
| C、乙醇中的乙酸(NaOH溶液 分液) |
| D、苯中的溴:(NaOH溶液 分液) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com