
用铅蓄电池电解饱和食盐水制取氯气,已知铅蓄电池放电时发生如下反应:
负极:Pb+SO42——2e—==PbSO4
正极:PbO2+4H++SO42—+2e—==PbSO4+2H2O
若制得Cl20.050mol,电池内消耗的H2SO4的物质的量至少是
A、0.025mol B、0.050mol
C、0.10mol D、0.20mol
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015江苏省宿迁市五校高一上学期期中联考化学试卷(解析版) 题型:选择题
氮化铝 (AlN)广泛应用于电子、陶瓷等工业领域。在一定条件下,AlN可通过反应Al2O3 + N2 + 3C 2AlN + 3CO合成。下列叙述正确的是
2AlN + 3CO合成。下列叙述正确的是
A.该反应中氧化剂与还原剂物质的量之比为3:1
B.AlN是还原产物
C.AlN的摩尔质量为41g
D.上述反应中,每生成lmolAlN需转移6mol电子
查看答案和解析>>
科目:高中化学 来源:2014-2015安徽省蚌埠市高一上学期期中化学试卷(解析版) 题型:实验题
(8分)实验室要用98%(ρ=1.84 g·cm-3)的硫酸配制3.68 mol·L-1的硫酸溶液400mL
(1)计算所需98%的硫酸 mL
(2)该实验中除了要用到量筒、烧杯以外,还需要用到的玻璃仪器(无需装瓶)有: 、 、 。
(3)若配制3.68mol·L-1的硫酸溶液的其他操作均正确,但出现下列错误操作,将导致所配制的硫酸溶液浓度偏低的是 。
A、浓硫酸溶解后未冷却,直接转移至容量瓶后定容
B、将烧杯内的稀硫酸向容量瓶中转移时,因操作不当使部分稀硫酸溅出瓶外
C、用量筒量取浓硫酸时,俯视读数
D、容量瓶使用前用3.68mol·L-1硫酸的溶液润洗
查看答案和解析>>
科目:高中化学 来源:2014-2015安徽省蚌埠市高一上学期期中化学试卷(解析版) 题型:选择题
下列各组中的两物质作用时,改变反应条件或反应物用量对生成物没有影响的是
A、Na2O2和CO2 B、Na和O2 C、NaOH和CO2 D、C和O2
查看答案和解析>>
科目:高中化学 来源:2014-2015安徽省高二上学期第一次质量检测化学试卷(解析版) 题型:填空题
(6分)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g)ΔH=-574 kJ·mol-1
CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g)ΔH=-1 160 kJ·mol-1
若用标准状况下4.48 L CH4还原NO2至N2,整个过程中转移电子总数为______(阿伏加德罗常数的值用NA表示),放出的热量为______kJ。
查看答案和解析>>
科目:高中化学 来源:2014-2015安徽省高二上学期第一次质量检测化学试卷(解析版) 题型:选择题
烧杯A中盛放0.1 mol·L-1的H2SO4溶液,烧杯B中盛放0.1 mol·L-1的CuCl2溶液(两种溶液均足量),装置如图所示,
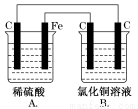
下列说法正确的是
A.A为电解池,B为原电池
B.Fe电极发生还原反应
C.当A烧杯中产生0.1 mol气体,B烧杯中产生气体也为0.1 mol
D.一段时间后,B烧杯中溶液的浓度增大
查看答案和解析>>
科目:高中化学 来源:2014-2015安徽省高二上学期第一次质量检测化学试卷(解析版) 题型:选择题
下列说法正确的是
A.热化学方程式中,若没有注明温度和压强,则表示反应热在标准状况下测得的数据
B.升高温度或加入催化剂,都可以改变化学反应的反应热
C.据能量守恒定律,反应物的总能量一定等于生成物的总能量
D.物质发生化学变化一定伴随着能量变化
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省绥化市三校高二上学期期中化学试卷(解析版) 题型:选择题
某温度下,体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g)  Z(g)+W(s) ΔH>0下列叙述正确的是
Z(g)+W(s) ΔH>0下列叙述正确的是
A.加入少量W,逆反应速率增大
B.升高温度,平衡逆向移动
C.当容器中气体压强不变时,反应达到平衡
D.平衡后加入X,上述反应的ΔH增大
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省哈尔滨市高二10月月考化学试卷(解析版) 题型:选择题
如果25 ℃时,Kw=1.0×10-14,某温度下Kw=1.0×10-12。这说明
A.某温度下的电离常数较大
B.前者的c(H+)较后者大
C.水的电离过程是一个放热过程
D.Kw和K电离无直接关系
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com