
分析 取代反应是有机物中的原子或原子团被其他的原子或原子团所代替生成新的化合物的反应;
氧化反应是物质所含元素化合价升高的反应;
加成反应是有机物分子中的不饱和键断裂,断键原子与其他原子或原子团相结合,生成新的化合物的反应;
聚合反应是由单体合成聚合物的反应过程,以此解答该题.
解答 解:①由乙炔制取氯乙烯:乙炔与氯化氢发生加成反应生成氯乙烯,属于加成反应;
②乙烷在空气中燃烧:乙烷的燃烧属于氧化反应;
③乙烯使溴的四氯化碳溶液褪色:乙烯分子中含有碳碳双键,能够与溴发生加成反应;
④乙烯使酸性高锰酸钾溶液褪色:乙烯中官能团碳碳双键被酸性高锰酸钾溶液氧化,该反应为氧化反应;
⑤由乙烯制取聚乙烯:乙烯通过加聚反应生成聚乙烯,属于聚合反应;
⑥甲烷与氯气在光照的条件下反应:甲烷中氢原子被氯原子取代,该反应为取代反应;
⑦由乙烯制取乙醇:乙烯与水发生加成反应生成乙醇,该反应为加成反应;
根据以上分析可知,属于取代反应的是:⑥;属于氧化反应的是:②④;
属于聚合反应的是:⑤,故答案为:⑥;②④;⑤.
点评 本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握有机物官能团的性质以及反应类型的判断,难度不大.


 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:解答题
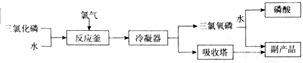
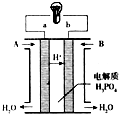
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
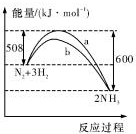
| A. | 该反应的热化学方程式为:2NH3?N2+3H2△H=-92kJ.mol-1 | |
| B. | 生成物的能量之和比反应物的能量之和高 92 kJ | |
| C. | a曲线是未加入催化剂时的能量变化曲线 | |
| D. | 加入催化剂可增加正反应速率,减小逆反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Li在N2中燃烧生成Li3N | |
| B. | LiOH是极易溶的强碱 | |
| C. | Be(OH)2既能溶于强酸又能溶于强碱溶液 | |
| D. | 硼酸钠溶液显碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
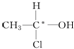 等,下列化合物中存在对映异构体的是( )
等,下列化合物中存在对映异构体的是( )| A. | 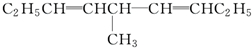 | B. | 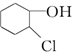 | ||
| C. | 甲酸 | D. | C6H5CH2OCH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 燃烧产物只有CO2和H2O | B. | 与卤素单质发生取代反应 | ||
| C. | 都溶于水 | D. | 通常不与强酸、强碱、强氧化剂反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{8}^{16}$O和${\;}_{8}^{18}$O的质子数相同 | |
| B. | ${\;}_{8}^{16}$O2和${\;}_{8}^{18}$O2互为同素异形体 | |
| C. | ${\;}_{8}^{16}$O和${\;}_{8}^{18}$O中子数相差2 | |
| D. | ${\;}_{8}^{17}$O原子核内中子数与核外电子数之差为1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
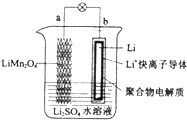
| A. | a为电池的正极 | B. | 放电时,b极电极反应式:Li-e-=Li+ | ||
| C. | 放电时,a极锂的化合价发生变化 | D. | 放电时,溶液中Li+从b向a迁移 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
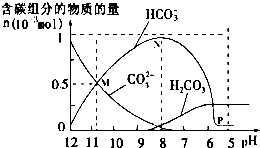 25℃时在10mL 0.1mol•L-1Na2CO3溶液中逐滴加入0.1mol•L-1HCl溶液20mL,溶液中部分含碳微粒的物质的量随溶液pH的变化如图所示.下列说法不正确的是( )
25℃时在10mL 0.1mol•L-1Na2CO3溶液中逐滴加入0.1mol•L-1HCl溶液20mL,溶液中部分含碳微粒的物质的量随溶液pH的变化如图所示.下列说法不正确的是( )| A. | HCl溶液滴加一半时,溶液pH>7 | |
| B. | 当溶液的pH=8时,溶液中NaHCO3的物质的量浓度为0.1mol•L-1 | |
| C. | 0.1 mol•L-1Na2CO3溶液中c(Na+)+c(H+)=c(OH-)+2c(CO32-)+c(HCO3-) | |
| D. | 在M点:c(Na+)>c(CO32-)=c(HCO3-)>c(OH-)>c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com