
| A�� | Ҫ���ʵ�����ȡ10.6gNa2CO3•10H2O���� | |
| B�� | ���ݺ������ƿ��תҡ�ȣ�����Һ����ڿ̶ȣ��ٲ��伸��ˮ���̶��ߣ��ᵼ����ҺŨ��ƫ�� | |
| C�� | ����ʱ������ƿ�����������������ˮ�ᵼ��Ũ��ƫ�� | |
| D�� | ����ʱ���ӿ̶��ᵼ��Ũ��ƫ�� |
���� A������m=CVM������Ҫ���ʵ�������
B����������һ�����ʵ���Ũ����Һ�IJ���ѡ��������
C������ʱ����Ҫ������ƿ�м�������ˮ��
D������ʱ���ӿ̶��ߣ�������Һ���ƫС��
��� �⣺A������1mol/L��Na2CO3��Һ100mL����Ҫ̼���ƾ��������m=1mol/L��286g/mol��0.1L=28.6g����A����
B������һ�����ʵ���Ũ����Һ���ƵIJ��裺�������ܽ⡢��Һ��ϴ�ӡ����ݵȣ��õ�����������ƽ��ҩ�ס����������ձ���100mL����ƿ����ͷ�ιܣ���B����
C������ʱ����Ҫ������ƿ�м�������ˮ����������ʱ������ƿ�����������������ˮ������ҺŨ����Ӱ�죬��C����
D������ʱ���ӿ̶��ߣ�������Һ���ƫС������C=$\frac{n}{V}$��֪��ҺŨ��ƫ�ߣ���D��ȷ��
��ѡ��D��
���� ���⿼����һ�����ʵ���Ũ����Һ�����ƣ���Ϥ���ƹ����ǽ���ؼ���ע������C=$\frac{n}{V}$�������ķ�������Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
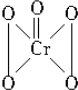
| A�� | ȫ��-1�� | B�� | $\frac{4}{5}$Ϊ-1�ۣ�$\frac{1}{5}$Ϊ-2�� | ||
| C�� | ȫ��-2�� | D�� | $\frac{4}{5}$Ϊ-2�ۣ�$\frac{1}{5}$Ϊ-1�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��� | �¶� | 0.1mol•L-1Na2S2O3��Һ | 0.1mol•L-1H2SO4��Һ | H2O | �ﵽ��ͬ�̶����õ�ʱ��/s |
| �� | 25�� | 25mL | 25mL | 0mL | 4 |
| �� | 25�� | 25mL | 15mL | 10.0mL | 6 |
| �� | 25�� | V1 | 25mL | 10mL | 6 |
| �� | 45�� | V2 | 25mL | V3 | 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���߲������������� | B�� | ǿ����Һ�����������ٶȿ� | ||
| C�� | ������Һ�����϶������ | D�� | ���Ƚ����߲����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������Ư�۴�������ˮ�����ߵ�����ԭ����ͬ | |
| B�� | ��������10mL pH=3�Ĵ�����Һ�м�ˮϡ�ͺ���Һ��$\frac{c��C{H}_{3}CO{O}^{-}��}{c��C{H}_{3}COOH��•c��O{H}^{-}��}$���� | |
| C�� | ��ˮ����ˮ����ˮ�ǻ���ˮ����ˮ�����Ǵ����� | |
| D�� | ���ó����ʯ��ˮ����̼���ƺ�̼������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
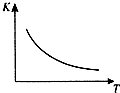 ��ҵ���Ʊ�H2��һ����Ҫ�����ǣ�CO��g��+H2O��g��?CO2 ��g��+H2��g����H=Q kJ/mol����֪�÷�Ӧ��ƽ�ⳣ��K���¶�T�Ĺ�ϵ��ͼ��ʾ������һ�̶��ݻ����ܱ������У�850��ʱ����������Ӧ����������ڸ����ʵ�Ũ�� ��mol/L����ʱ��ı仯��ϵ�������֪��850��ʱ�÷�Ӧ�Ļ�ѧƽ�ⳣ��K=1.0����ش��������⣺
��ҵ���Ʊ�H2��һ����Ҫ�����ǣ�CO��g��+H2O��g��?CO2 ��g��+H2��g����H=Q kJ/mol����֪�÷�Ӧ��ƽ�ⳣ��K���¶�T�Ĺ�ϵ��ͼ��ʾ������һ�̶��ݻ����ܱ������У�850��ʱ����������Ӧ����������ڸ����ʵ�Ũ�� ��mol/L����ʱ��ı仯��ϵ�������֪��850��ʱ�÷�Ӧ�Ļ�ѧƽ�ⳣ��K=1.0����ش��������⣺| ʱ��/min | CO��g�� | H2O��g�� | CO2��g�� | H2��g�� |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c4 |
| 4 | c1 | c2 | c3 | c4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ݢڢ٢ܢ� | B�� | �ݢ٢ڢۢ� | C�� | �ܢۢڢ٢� | D�� | �ܢۢ٢ڢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com