
【题目】A、B、C、D、E、F、G均是原子序数小于36的元素.A的基态原子外围电子排布式为3s2;B原子的L电子层的P能级上有一个空轨道; C元素的基态原子最外层有3个未成对电子,次外层有2个电子; D 的原子的2p轨道上有1个电子的自旋方向与其它电子的自旋方向相反;E是海水中除氢、氧元素外含量最多的元素;F和G在周期表中既处于同一周期又位于同一族,且原子序数F比G小2. 根据信息回答下列问题:
(1)C的外围电子排布图为 . C与氢元素可分别形成含10个电子的分子、阴离子和阳离子,阳离子中中心原子的杂化类型为
(2)用电子式表示化合物AE2的形成过程
(3)F与BD易形成配合物F(BD)5 , 在F(BD)5中F的化合价为
(4)E有多种含氧酸根①EO﹣②EO2﹣③EO3﹣④EO4﹣ , 其中空间构型为四面体形的是(填序号).
(5)C 的最高价氧化物对应的水化物与A 的单质反应时,C被还原到最低价,该反应的化学方程式为 .
【答案】
(1)![]() ; sp3
; sp3
(2)![]()
(3)0
(4)④
(5)4Mg+10HNO3=4Mg(NO3)2+NH4NO3+3H2O
【解析】解:(1)C为氮元素,它的外围电子排布图为 ![]() ,C与氢元素的阳离子为铵根离子,中心原子氮的价层电子对数为
,C与氢元素的阳离子为铵根离子,中心原子氮的价层电子对数为 ![]() =4,所以氮原子的杂化类型为sp3杂化,所以答案是:
=4,所以氮原子的杂化类型为sp3杂化,所以答案是: ![]() ;sp3;(2)AE2为MgCl2,用电子式表示MgCl2的形成过程为
;sp3;(2)AE2为MgCl2,用电子式表示MgCl2的形成过程为 ![]() ,
,
所以答案是: ![]() ;(3)F(BD)5为Fe(CO)5,因为Fe(CO)5化合价的代数和为0,CO的化合价的代数和为0,则Fe元素的化合价为0,所以答案是:0;(4)Cl有多种含氧酸根①ClO﹣②ClO2﹣③ClO3﹣④ClO4﹣,中心原子Cl的价层电子对数都为
;(3)F(BD)5为Fe(CO)5,因为Fe(CO)5化合价的代数和为0,CO的化合价的代数和为0,则Fe元素的化合价为0,所以答案是:0;(4)Cl有多种含氧酸根①ClO﹣②ClO2﹣③ClO3﹣④ClO4﹣,中心原子Cl的价层电子对数都为 ![]() =4,氯原子都是按sp3方式杂化的,其中只有ClO4﹣,有四个Cl﹣O键,没有孤电子对,其空间构型为四面体型,其它含氧酸根都有孤电子对,空间构型不为四面体,所以答案是:④;(5)C 的最高价氧化物对应的水化物与A 的单质反应时,C被还原到最低价,生成硝酸铵,该反应的化学方程式为4Mg+10HNO3=4Mg(NO3)2+NH4NO3+3H2O,
=4,氯原子都是按sp3方式杂化的,其中只有ClO4﹣,有四个Cl﹣O键,没有孤电子对,其空间构型为四面体型,其它含氧酸根都有孤电子对,空间构型不为四面体,所以答案是:④;(5)C 的最高价氧化物对应的水化物与A 的单质反应时,C被还原到最低价,生成硝酸铵,该反应的化学方程式为4Mg+10HNO3=4Mg(NO3)2+NH4NO3+3H2O,
所以答案是:4Mg+10HNO3=4Mg(NO3)2+NH4NO3+3H2O.


 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:高中化学 来源: 题型:
【题目】现有5瓶失去标签的液体,已知它们可能是乙醇、乙酸、苯、乙酸乙酯、葡萄糖中的一种。现通过如下实验来确定各试剂瓶中所装液体的名称:
实验步骤和方法 | 实验现象 |
①把5瓶液体分别依次标号A、B、C、D、E,然后闻气味 | 只有E没有气味 |
②各取少量于试管中 ,加水稀释 | 只有C、D不溶解而浮在水面上 |
③分别取少量5种液体于试管中,加新制Cu(OH)2并加热 | 只有B使沉淀溶解,E中产生砖红色沉淀 |
④各取C、D少量于试管中,加稀NaOH溶液并加热 | 只有C仍有分层现象,且在D的试管中闻到特殊香味 |
(1)写出这6种物质的名称。
A____________ B____________ C____________ D____________ E____________
(2)在D中加入NaOH溶液并加热的化学方程式为__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为周期表中短周期的一部分,W、X、Y、Z四种元素最外层电子数之和为24。下列说法正确的是
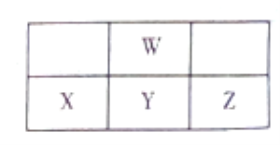
A. X、Y、Z的含氧酸的酸性依次增强
B. W元素形成的单核阴离子还原性强于X
C. Y、W形成的化合物一定能使酸性KMnO4溶液褪色
D. W与氢元素形成的化合物中可能含有非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述与图象对应符合的是( ) 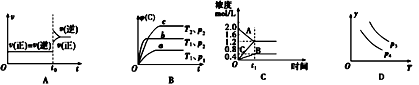
A.对于达到平衡状态的N2(g)+3H2(g)2NH3 (g)在t0时刻充入了一定量的NH3 , 平衡逆向移动
B.对于反应 2A(g)+B(g)C(g)+D(g)△H<0,p2>p1 , T1>T2
C.该图象表示的化学方程式为:2A═B+3C
D.对于反应 2X(g)+3Y(g)2Z(g)△H<0,y可以表示Y的百分含量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据20℃时某些物质的溶解度(g)数据:
CaCO3 | CaSO4 | Mg(OH)2 | MgCO3 |
1.4×10﹣3 | 2.55×10﹣2 | 9×10﹣4 | 1.1×10﹣2 |
下列说法不正确的是( )
A.硫酸钙悬浊液中存在CaSO4(s)Ca2+(aq)+SO42﹣(aq)
B.用Na2CO3溶液浸泡锅炉中的水垢,可将水垢中的CaSO4转化为CaCO3
C.向Mg(OH)2悬浊液中滴加FeCl3 , 沉淀变为红褐色,说明溶解度Fe(OH)3<Mg(OH)2
D.向2ml饱和MgCl2 溶液中先后滴加0.1mol/L的Na2CO3、NaOH溶液各2滴,产生的白色沉淀为Mg(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以有机物A合成聚酯类高分子化合物F的路线如下图所示:

已知:RCH=CH3 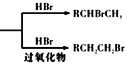
(1)A、C中含氧官能团的名称分别为_______,A生成B的反应类型为_________。
(2)D与NaOH水溶液反应的化学方程式为_________________________________。
(3)①E生成F的化学方程式为_____________________________________________。
②若F的平均相对分子质量为20000,则其平均聚合度为_____(填字母代号)。
A.54 B.108 C.119 D.133
(4)E在一定条件下还可以合成含有六元环结构的G,则G的结构简式为____________。
(5)满足下列条件的C的同分异构体有____种(不考虑立体异构)。
①含有1个六元碳环,且环上相邻4个碳原子上各连有一个取代基
②1mol该物质与新制氢氧化铜悬浊液反应产生2mol砖红色沉淀
(6)写出以![]() 为原料(其他试剂任选)制备化合物
为原料(其他试剂任选)制备化合物![]() 的合成路线,请用以下方式表示:
的合成路线,请用以下方式表示: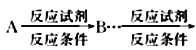 目标产物。__________________
目标产物。__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是( )
A.棉花和蚕丝的主要成分是纤维素
B.蛋白质在一定条件下可以发生水解生成葡萄糖
C.煤的气化是在高温下煤和水蒸汽作用转化为可燃性气体的过程
D.油脂的主要成分是高级脂肪酸甘油酯,在碱性条件下水解可以得到高级脂肪酸和甘油
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图A所示的转化关系中(具体反应条件略),a、b、c和d分别为四种短周期元素的常见单质,其余均为它们的化合物,i的溶液为常见三大强酸,a的一种同素异形体的晶胞如图B(正四面体立体网状结构)所示. 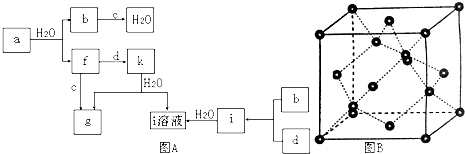
回答下列问题:
(1)图B对应的物质名称是 ,
(2)d中元素的原子核外电子排布式为 .
(3)图A中由二种元素组成的物质中,沸点最高的是 , 原因是 , 该物质的分子构型为 .
(4)图A中的双原子分子中,极性最大的分子是 .
(5)k的分子式为 , 中心原子的杂化轨道类型为 , 属于分子(填“极性”或“非极性”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素a、b、c、d、e,其原子半径与原子序数的关系如图,下列说法错误的是
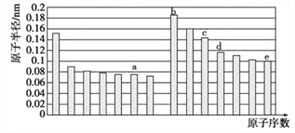
A. c元素的离子半径比e的离子半径小
B. d元素对应的最高价氧化物的水化物酸性比e元素弱
C. b、c、d三种元素对应的最高价氧化物的水化物相互间能发生反应
D. a与b两种元素可形成既有离子键又有非极性共价键的化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com