

分析 海带在坩埚中灼烧,海带灰浸泡后,过量除去杂质,含碘离子溶液加入二氧化锰,在酸性条件下发生氧化还原反应生成碘,⑤为萃取操作,用于分离碘,含碘苯溶液蒸馏可得到碘,以此解答该题.
解答 解:(1)步骤②的实验操作用于溶解固体药品,选用仪器的名称是烧杯、玻璃棒,步骤⑥的目的是从含碘CCl4溶液中分离出单质碘和回收CCl4,为蒸馏操作,
故答案为:烧杯、玻璃棒;蒸馏;
(2)步骤⑤为萃取,引用四氯化碳,酒精易溶于水,不能用作萃取剂,故答案为:酒精溶于水而CCl4不溶于水;
(3)反应MnO2+2KI+2H2SO4═MnSO4+K2SO4+2H2O+I2中,Mn元素化合价由+4价降低到+2价,I元素化合价由-1价升高到0价,反应的离子方程式为MnO2+2I-+4H+═Mn2++2H2O+I2,用双线桥标出电子转移方向和数目为 ,
,
故答案为: ;MnO2+2I-+4H+═Mn2++2H2O+I2.
;MnO2+2I-+4H+═Mn2++2H2O+I2.
点评 本题考查海水资源的综合利用,为高频考点,侧重于学生的分析、实验能力的考查,侧重考查物质的检验、混合物的分离和提纯,明确常见混合物分离和提纯方法及其选取方法是解本题关键,难度不大.


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 纯净物 | 混合物 | 电解质 | 非电解质 | |
| A | 盐酸 | 冰水混合物 | 小苏打 | 干冰 |
| B | 蒸馏水 | 氨水 | 火碱 | 二氧化硫 |
| C | 硫酸 | 胆矾 | 纯碱 | 氨气 |
| D | 硝酸 | 食盐 | 氢氧化钠溶液 | 生石灰 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相对分子质量 M=$\frac{22.4mw}{[(1-w)V]}$ | B. | 物质的量浓度 c=$\frac{1000dV}{(MV+22.4m)}$ | ||
| C. | 溶质的质量分数 w=$\frac{MV}{22.4m}$ | D. | 溶液密度 d=$\frac{cM}{1000w}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
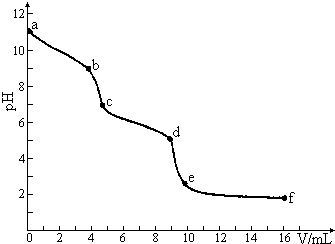 常温下,用已知浓度的盐酸滴定未知浓度的Na2CO3溶液.用 pH传感器测得混合溶液的pH变化曲线如下图(已知:饱和CO2溶液的pH为5.6),下列说法正确的是 ( )
常温下,用已知浓度的盐酸滴定未知浓度的Na2CO3溶液.用 pH传感器测得混合溶液的pH变化曲线如下图(已知:饱和CO2溶液的pH为5.6),下列说法正确的是 ( )| A. | 该Na2CO3溶液的浓度为0.001mol/L | |
| B. | 在pH=7时,c(Na+)=c(Cl-) | |
| C. | 在pH=6时,c(Na+)>c(HCO3-)>c(CO32-) | |
| D. | c→d发生的主要离子反应为:CO32-+H+=HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3个 | B. | 4个 | C. | 5个 | D. | 6个 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com