
���й��ڵ������Һ�����ӹ�ϵ��˵����ȷ����
A��0.1mol��L��1NaHCO3��Һ������Ũ�ȹ�ϵ��c(Na��)��2c(CO32-)��c(HCO3-)��c(H2CO3)
B��0.1mol��L��1NH4Cl��0.1mol��L��1NH3��H2O�������Ϻ�����Ũ�ȹ�ϵ��c(Cl��)��c(NH4+)��c(H��)��c(OH��)
C�������£����������Һ�еμ���������ʹ��Һ��pH��7��������Һ�У�c(Na��)��c(CH3COO��)
D�������£���pH��1����Һ�У�Fe2����NO3-��ClO����Na���ܴ�������
C
��������
���������A�������غ㣬Ӧ���ǣ�c(Na��)��c(CO32-)��c(HCO3-)��c(H2CO3)������NH3��H2O�ĵ���̶ȴ��� NH4+��ˮ��̶ȣ���Һ�Լ��ԣ�����Ũ�ȹ�ϵӦ����c(NH4+)��c(Cl��) ��c(OH��) �� c(H��)��B����C�и��ݵ���غ�c(Na��)+ c(H��)��c(CH3COO��)+ c(OH��)����Һ�����ԣ�c(OH��) =c(H��)����c(Na��)��c(CH3COO��)���ԣ�D. Fe2���л�ԭ�ԣ�ClO������ǿ�����ԣ����ܴ������棬����
���㣺���ӵ�Ũ�ȴ�С�ȽϺ����ӹ������⡣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ɽ��ʡ�����и�һ��ѧ������ĩͳ����ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ��д��ȷ����
A��Cl2ͨ��ˮ�У�
B��NaHCO3��Һ�еμ����
C���Ƽ���ˮ�У�
D��ͭƬ����HNO3ϡ��Һ�У�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015���Ļ�������������һ�и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NAΪ�����ӵ�������������������ȷ����
A��3molNO2������������ˮ�г�ַ�Ӧת�Ƶĵ�������Ϊ2NA
B��7.8g Na2O2�����к��е���������Ϊ0.4NA
C����״����,11.2L��SO3������ˮ��ַ�Ӧ���ɵ���Һ��H+������ΪNA
D��0.5molNa��������������ȼ������Na2O2��Na2O���õ��ĵ�������Ϊ0.5NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015���Ļ�������������һ�и߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ʵ���Ũ�Ⱦ�Ϊ0.01 mol��L��1�Ģ�NaHCO3����Na2CO3����CH3COOH����CH3COONa ������Һ������˵����ȷ����
A���ٵ�����Ũ��Ϊ��c(Na��)>c(OH��)>c(HCO3-)>c(H��)
B���������¶ȣ� ��С
��С
C���ۼ���������ˮϡ�ͣ�����ƽ�������ƶ���c(H��)����
D���ܺ͢۵������ϣ���ҺpH<7��c(CH3COO��)��c(OH��)>c(CH3COOH)��c(H��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015���Ļ�������������һ�и߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A��ԭ�Ӻ�������Ų�ʽΪ1s2��ԭ����ԭ�Ӻ�������Ų�ʽΪ1s22s2��ԭ�ӻ�ѧ��������
B��Fe3+�����������Ų�ʽΪ3s23p63d5
C����̬ͭԭ�ӵ������ĵ����Ų�ͼ: 
D�����зǽ���Ԫ�ض��ֲ���p��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015���Ļ�������������һ�и߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��һ�������£�Na2CO3��Һ����ˮ��ƽ�⣺CO32����H2O HCO3����OH��������˵����ȷ����
HCO3����OH��������˵����ȷ����
A��ϡ����Һ��ˮ��ƽ�ⳣ������
B��ͨ��CO2��ƽ��������Ӧ�����ƶ�
C�������¶ȣ� ��С
��С
D������NaOH���壬��ҺpH��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�����и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ������
��10�֣�������ͭ(Cu2O)��һ���ʺ�ɫ��ĩ״���壬����������ˮ������������Һ�з�����Ӧ�������ᡢ���ᡢ���ᷴӦ���£�
��Cu2O+H2SO4 = CuSO4 +Cu+H2O
��Cu2O+ 4HCl = 2HCuCl2 + H2O
��3Cu2O + 14HNO3(ϡ) = 6Cu(NO3)2 + 2NO��+ 7H2O
��1��Cu2O��Cu�Ļ��ϼ�Ϊ_____________��
��2����Ӧ����������Ϊ____________����ԭ��Ϊ___________��
��3����Ӧ��_________����ǡ����ǡ���������ԭ��Ӧ��������˵��ת�Ƶ����������������˵���ж�����_______________________��
��4����д����Ӧ�۵����ӷ���ʽ________________________�����ɱ�״����22.4L NO��ת�Ƶ�����Ϊ_________��������������������ʵ���Ϊ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�����и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����������ȷ����
A��3.01��1023��SO2���ӵ�����Ϊ32 g
B��CH4��Ħ������Ϊ16 g
C��1 mol H2O������Ϊ18 g/mol
D����ͬ�����壬��������ȣ������������ķ�����һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�����и߶���ѧ����ĩ���Ի�ѧ�������Ծ��������棩 ���ͣ�ѡ����
��ͼ�ǵ��CuCl2��Һ��װ�ã�����c��dΪʯī�缫���������йص��ж���ȷ����
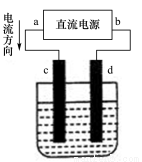
A���������У�d�缫��������
B��dΪ�������缫��ӦΪ��2Cl‑ - 2e- = Cl2��
C��a������b����
D���������У�������Ũ�Ȳ���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com