
| A. | ②④ | B. | ②③ | C. | ①③ | D. | ①④ |
分析 根据乙醇沸点低,易挥发,故可以易被检测及乙醇具有还原性,K2Cr2C7具有强氧化性,可以氧化乙醇,自身生成Cr3+来分析解答.
解答 解:①乙醇沸点低,易挥发,若饮酒,呼出的气体中含有酒精,与测定原理有关;
②乙醇密度比水小,可与水以任意比混溶,与测定原理无关;
③乙醇分子中含有羟基,具有还原性,K2Cr2C7具有强氧化性,可以把乙醇迅速氧化为乙酸蓝绿色的Cr3+,与测定原理有关;
④乙醇可看成是乙烷中的氢原子被羟基取代后的产物,是烃的含氧化合物,与测定原理无关;
故对乙醇的描述与此测定原理有关的是①③;
故选C.
点评 本题主要考查乙醇的性质,难度不大,本题中的信息交警对驾驶员进行呼气酒精检测的原理是解答的关键,学生应学会信息的抽取和应用来解答习题.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
 现有丙炔和氢气的混合气体5L,其中氢气在混合气体中的体积分数为x,在催化剂作用下,经充分反应后得到的气体的体积为V L(所有体积均在同温同压下测定).
现有丙炔和氢气的混合气体5L,其中氢气在混合气体中的体积分数为x,在催化剂作用下,经充分反应后得到的气体的体积为V L(所有体积均在同温同压下测定).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
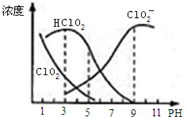 亚氯酸钠是一种高效氧化剂漂白剂,主要用于 棉纺、亚麻、纸浆等漂白亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2是有毒气体.经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出).则下列分析不正确的是( )
亚氯酸钠是一种高效氧化剂漂白剂,主要用于 棉纺、亚麻、纸浆等漂白亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2是有毒气体.经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出).则下列分析不正确的是( )| A. | 亚氯酸钠在碱性条件下较稳定 | |
| B. | 25℃时,HClO2的电离平衡常数的数值Ka=10-6 | |
| C. | 使用该漂白剂的最佳pH为3 | |
| D. | 25℃时,同浓度的HClO2溶液和NaClO2溶液等体积混合,则混合溶液中有c(HClO2)+2c(H+)=c(ClO2-)+2c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | F | Ne | |||
| 3 | Na | Al | P | S | Cl |
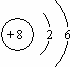 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ②④⑥ | C. | ②③④ | D. | ①③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烯 | B. | 1,3-丁二烯 | C. | 丙炔 | D. | 2-丁烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.061 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | 氢化物的稳定性为H2T<H2R | |
| B. | 单质与稀盐酸反应难易程度为L<Q | |
| C. | M与T形成的化合物能与氢氧化钠反应 | |
| D. | L2+与R2-的核外电子数相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com