



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
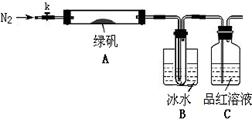
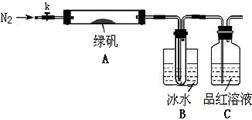
| A��ԭ�������CuO��Fe2O3���ʵ����ı�Ϊ1��2 |
| B��ԭ�������CuO��Fe2O3��������Ϊ2��1 |
| C������CO2����Һ��һ����Ba(HCO3)2 |
| D����Ӧ�����ɵ�CO2���Ϊ1.792 L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
| A��пͭԭ�����ͭ������ | B���õ�ⷨ����ͭʱ��ͭ������ |
| C���ڶƼ��϶�ͭʱͭ���Դ�������� | D��ͭ������ʱ��һ���ܽ� |
|
 ��ʵ����̡�
��ʵ����̡��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| ѡ�� | ʵ�� | ���� | ���ͻ���� |
| A | ����FeCl3���� | ��Һ��ɺ��ɫ | FeCl3��ˮ��̶ȱ�� |
| B | ��������ˮ | ��Һ��ɫ��dz | c(Fe3��)��С |
| C | ��������Fe�� | ��Һ��ɫ���dz��ɫ | 2Fe3����Fe=3Fe2�� |
| D | ��FeCl3��Һ�� | ��Һ��ɺ��ɫ | ˮ�ⷴӦ��H>0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

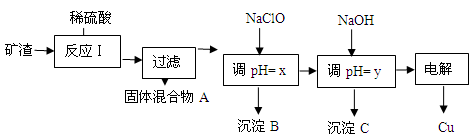
| ������ | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
| ��ʼ����pH | 5.4 | 4.0 | 1.1 | 5.8 |
| ������ȫpH | 6.7 | 5.2 | 3.2 | 8.8 |
 HClO��ClO������H+���Ӷ��ﵽ����pH��Ŀ��
HClO��ClO������H+���Ӷ��ﵽ����pH��Ŀ�� HClO+OH����OH������H+ ���Ӷ��ﵽ����pH��Ŀ��
HClO+OH����OH������H+ ���Ӷ��ﵽ����pH��Ŀ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
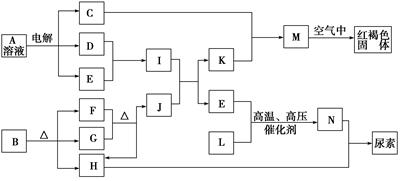
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
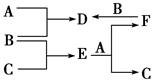
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ֻ�Тٻ�� | B��ֻ�Тڻ�� |
| C��ֻ�Тٻ�ڻ�� | D��������������������һ�� |
�鿴�𰸺ͽ���>>
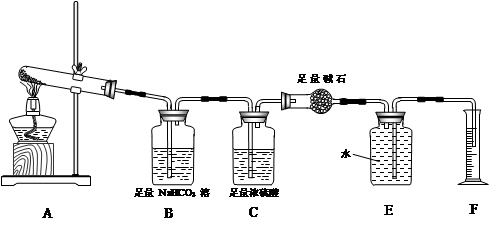
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
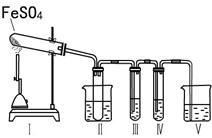
| A��2 mol/LNa2CO3��Һ |
| B��Ʒ����Һ |
| C��0.5 mol/LBaCl2��Һ |
| D��0.5 mol/LBa(NO3)2 |
| �������� | Ԥ��ʵ������ | Ԥ��ʵ����� |
| ������һ����Һ�м��� �� | | �����к���Fe2O3 |
| ����һ����Һ�еμ�2�λ�ɫK3[Fe(CN)6]��Һ�� | ������ɫ���� | |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com