

分析 铬铁矿(主要成分:FeO•Cr2O3,还含有少量的Al2O3)氧化后亚铁离子被氧化为铁离子,铬离子被氧化为+4价Na2CrO4,加入氢氧化钠溶液浸取,铁离子沉淀,氧化铝溶解生成偏铝酸钠,通过调节溶液PH,NaAlO2等杂质可以以沉淀的形式除去,水浸过滤后得到Na2CrO4溶液,加入硫酸酸化反应为:2Na2CrO4+H2SO4?Na2SO4+Na2Cr2O7+H2O,通过蒸发浓缩,冷却结晶,过滤洗涤得到晶体,以此解答该题.
解答 解:(1)①熔融状态下碳酸钠与二氧化硅等反应,可导致瓷坩埚炸裂,应在铁坩埚中进行,故答案为:铁;
②增大反应速率,可增大固体表面积、升高温度,由于为固体,则加入固体的量浓度不变,不影响速率,故答案为:AC;
(2)步骤II中加入NaOH溶液时氧化铝和氢氧化钠反应:2NaOH+Al2O3=2NaAlO2+H2O,除去氧化铝,NaAlO2等杂质可以以沉淀的形式除去,水浸过滤后得到Na2CrO4溶液,
故答案为:Al2O3+2NaOH=2NaAlO2+H2O;
(3)该步骤是CrO42-到Cr2O72-的转化,反应的离子方程式为:2CrO42-+2H+=Cr2O72-+H2O,现象是溶液由黄色变成橙色,
故答案为:2CrO42-+2H+=Cr2O72-+H2O;溶液由黄色变成橙色;
(4)NaCl的溶解度受温度影响小,K2Cr2O7的溶解度受温度影响大,分离NaCl、K2Cr2O7,将混合物溶解后,先蒸发浓缩析出NaCl,趁热过滤防止K2Cr2O7晶体,滤液经过冷却结晶、过滤得到K2Cr2O7晶体,
故答案为:②蒸发;③过滤;高温.
点评 本题考查物质制备实验,为高频考点,注意根据各问题进行分析解答,涉及化学反应速率影响因素、物质的分离提纯,注意理解利用溶解度进行物质的分离,充分考查学生的分析、理解能力及化学实验能力,难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫化钠的电子式: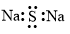 | |
| B. | HClO4的电离方程式:HClO4?H++ClO4- | |
| C. | 乙酸的结构简式:C2H4O2 | |
| D. | Mg2+的结构示意图: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 足量铁在氯气中反应,1mol铁失去的电子数为3NA | |
| B. | 6.4g Cu与足量硫充分反应后,转移电子数为0.2NA | |
| C. | 密闭容器中2mol NO与1mol O2充分反应后,产物的分子数为NA | |
| D. | 常温常压下,0.1mol NH3与0.1mol HCl充分反应后所得产物含0.1NA个分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
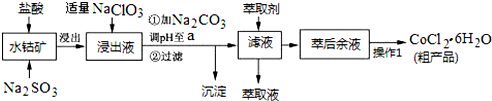
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
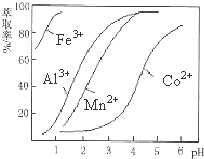
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
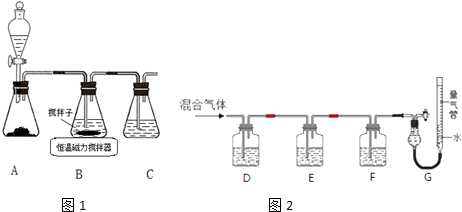
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
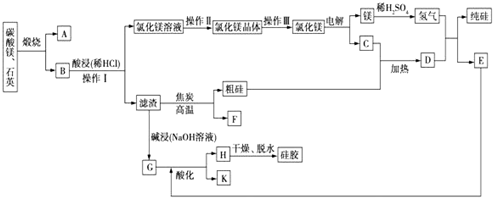
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 应量取的浓盐酸的体积/mL | 应选用的容量瓶的规格/mL | 除容量瓶外需要的其他仪器 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com