
现有常温条件下甲、乙、丙三种溶液,甲为0.1 mol/L的NaOH溶液,乙为0.1 mol/L的HCl溶液,丙为0.1 mol/L的CH3COOH溶液,试回答下列问题:
(1)甲溶液的pH=__________;
(2)丙溶液中存在电离平衡为______________________(用电离平衡方程式表示);
(3)甲、乙、丙三种溶液中由水电离出的c(OH-)的大小关系为________________________;
(4)某同学用甲溶液分别滴定20.00 mL乙溶液和20.00 mL丙溶液,得到如图所示两条滴定曲线,请完成有关问题:

①甲溶液滴定丙溶液的曲线是__________(填“图1”或“图2”);
②a=__________ mL。
解析:(1)c(OH-)=0.1 mol/L,
则c(H+)=10-13 mol/L,pH=13。
(2)CH3COOH溶液中存在CH3COOH和水的电离平衡。
(3)酸、碱对水的电离具有抑制作用,c(H+)或c(OH-)越大,水的电离程度越小,反之越大。
(4)氢氧化钠溶液滴定盐酸恰好中和时,pH=7;氢氧化钠溶液滴定醋酸恰好中和时,生成醋酸钠溶液,pH>7。对照题中图示,图2符合题意。a的数值是通过滴定管读数所确定的,因此读数应在小数点后保留两位。
答案:(1)13
(2)CH3COOH CH3COO-+H+
CH3COO-+H+
H2O OH-+H+
OH-+H+
(3)丙>甲=乙 (4)①图2 ②20.00


科目:高中化学 来源: 题型:
元素性质呈周期性变化的决定因素是
A.元素原子半径大小呈周期性变化
B.元素原子最外层电子排布呈周期性变化
C.元素的相对原子质量依次递增
D.元素的最高正化合价呈周期性变化
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图为对10 mL一定物质的量浓度的盐酸X用一定物质的量浓度的NaOH溶液Y滴定的图像,依据图像推出X和Y的物质的量浓度是下表内各组中的( )
如图为对10 mL一定物质的量浓度的盐酸X用一定物质的量浓度的NaOH溶液Y滴定的图像,依据图像推出X和Y的物质的量浓度是下表内各组中的( )
| A | B | C | D | |
| X/mol/L | 0.12 | 0.04 | 0.03 | 0.09 |
| Y/mol/L | 0.04 | 0.12 | 0.09 | 0.03 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 室温下,将1.000 mol/L盐酸滴入20.00 mL1.000 mol/L氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示。下列有关说法正确的是( )
室温下,将1.000 mol/L盐酸滴入20.00 mL1.000 mol/L氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示。下列有关说法正确的是( )
A.a点由水电离出的c(H+)=1.0×10-14 mol/L
B.b点:c(NH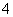 )+c(NH3·H2O)=c(Cl-)
)+c(NH3·H2O)=c(Cl-)
C.c点:c(Cl-)=c(NH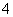 )
)
D.d点后,溶液温度略下降的主要原因是NH3·H2O电离吸热
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,可逆反应N2(g)+3H2(g)  2NH3(g)达到平衡的标志是 ( )
2NH3(g)达到平衡的标志是 ( )
A.N2 H2 NH3 的浓度相等
B.1个N≡N键断裂的同时,有6个N-H键形成
C.N2 H2 NH3的分子数比为1:3:2
D.单位时间消耗n mol N2 ,同时生成3n mol H2
查看答案和解析>>
科目:高中化学 来源: 题型:
把镁条投入到盛有盐酸的敞口容器里,产生H2的速率可由右图表 示。在下列因素中:①盐酸的浓度;②镁条的表面积;③溶液的温度; ④Cl-的浓度。影响反应速率的因素是 ( )
A. ①④ B.③④ C.①②③ D.②③

查看答案和解析>>
科目:高中化学 来源: 题型:
根据我省中心气象台报道,近年每到春季,我省沿海一些城市多次出现大雾天气,致使高速公路关闭,航班停飞。雾属于下列分散系中的 ( )
A.溶液 B.悬浊液 C.乳浊液 D.胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
下列推断正确的是
A.1 mol Na2O2与水反应,转移电子1 mol
B.Na2O、Na2O2组成元素相同,与CO2反应的产物也相同
C.钠能与氧气和水反应,钠暴露在空气中最终的产物是NaOH
D.将Na2O2加入酚酞试液中,得到红色溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com