
| A. | B3N3H6和苯是等电子体,B3N3H6分子中所有原子均不在同一平面上 | |
| B. | NO3-和CO32-是等电子体,均为平面正三角形结构 | |
| C. | H3O+和PCl3是等电子体,均为三角锥形 | |
| D. | CH4和NH4+是等电子体,均为正四面体形,键角均为60° |
分析 原子个数相同、最外层电子总数也相同的化合物是等电子体,等电子体具有相似的结构和性质.
解答 解:A.苯与B3N3H6价电子总数相等,原子数也相等互为等电子体,等电子体具有相似的结构,苯属于平面形结构,则B3N3H6分子各原子均在同一平面上,故A错误;
B.NO3-和CO32-价电子总数相等,原子数也相等互为等电子体,等电子体具有相似的结构,NO3-中心原子的价层电子对数=3+$\frac{1}{2}$(5+1-3×2)=3,没有孤电子对,空间构型为平面三角形,则CO32-为平面三角形,故B正确;
C.H3O+和PCl3价电子总数不等,不属于等电子体,故C错误;
D.CH4和NH4+是等电子体,均为正四面体形,但甲烷中四个H原子位于四个顶点,C原子位于四面体的中心,键角均为109°28ˊ,故D错误;
故选B.
点评 本题考查了等电子体,分子构型的判断,考查的知识点较多,难度较大,注意相关知识的积累.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知一个H2分子的体积是VL,则H2的摩尔体积是VNA L/mol | |
| B. | 肼(N2H4),熔点20℃,沸点113.5℃,标况下,11.2L肼的原子数小于3NA | |
| C. | 25℃、101KPa下,16gNH2-含有10NA个电子 | |
| D. | 标况下,4gH2、11.2LO2、1molSO3中O2体积最小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验内容 | 实验目的 | |
| A | 某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成 | 该溶液中含有SO42- |
| B | 向 AgCl和水的混合物滴加KI的溶液,产生黄色沉淀 | 验证溶解度AgI小于AgCl |
| C | 淀粉和稀硫酸混合加热后,加新制Cu(OH)2悬浊加热至沸腾 | 检验淀粉是否水解完全 |
| D | 向NaOH溶液中滴加FeCl3饱和溶液 | 制备Fe(OH)3胶体 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
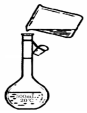 用胆矾晶体(CuSO4•5H2O )配制0.40mol/L的CuSO4溶液240mL,回答下列问题
用胆矾晶体(CuSO4•5H2O )配制0.40mol/L的CuSO4溶液240mL,回答下列问题查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某醋酸溶液的pH=a,将此溶液稀释1倍后,溶液的pH=b,则a>b | |
| B. | 在滴有酚酞溶液的氨水中,加入NH4Cl至溶液恰好无色,则此时溶液pH<7 | |
| C. | 若1mL pH=1的盐酸与100mL NaOH溶液混合后,溶液的pH=7,则NaOH溶液的pH=11 | |
| D. | 1.0×10-3mol•L-1盐酸的pH=3.0;1.0×10-8mol•L-1盐酸的pH=8.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 没有用蒸馏水洗烧杯2-3次,并将洗液移入容量瓶中 | |
| B. | 容量瓶刚用蒸馏水洗净,没有烘干 | |
| C. | 定容时,滴加蒸馏水,先使液面略高于刻度线,再吸出少量水使液面凹面与刻度线相切 | |
| D. | 定容时俯视刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L HF中含有的电子数为10NA | |
| B. | 在一定条件下,1molSO2和0.5molO2在密闭容器中充分反应,转移电子数目为2NA | |
| C. | 常温常压下,32gN2H4中含有的共价键数目为5NA | |
| D. | 某饱和FeCl3溶液中,若Fe3+的数目为NA,则Cl-的数目为3NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com