
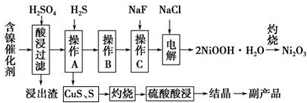
 为回收利用废镍催化剂(主要成分为NiO,另含Fe2O3、CaO、CuO、BaO等),科研人员研制了一种回收镍的新工艺.工艺流程如图:
为回收利用废镍催化剂(主要成分为NiO,另含Fe2O3、CaO、CuO、BaO等),科研人员研制了一种回收镍的新工艺.工艺流程如图:| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 7.7 |
| 沉淀完全的pH | 3.7 | 9.7 | 9.2 |
分析 (1)Fe2O3和硫酸反应生成盐和水,反应方程式为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(2)氧化钙和氧化钡与硫酸反应生成难溶的硫酸钙和硫酸钡;
(3)用氢氧化钠溶液调节溶液的pH值,容易引入杂质,所以方案是错误的;正确的操作应该是在调节pH前,应先在滤液中加入H2O2,使溶液中的Fe2+氧化为Fe3+;
(4)CuS、S灼烧后溶于稀硫酸中生成硫酸铜,所以副产品应该是胆矾;根据3Cu~2NO,3Cu2O~2NO,n(Cu)=0.1mol,n(NO)=0.1mol,可得混合物中Cu2O为0.05mol,故CuO为0.05mol.混合物中,0.1mol Cu不与稀H2SO4反应,0.05molCu2O、0.05molCuO与稀H2SO4反应,根据Cu2O、CuO中氧原子与H2SO4反应结合H+生成H2O,据此计算消耗硫酸;
(5)常温时CaF2的溶度积常数为2.7×10-11可知,溶液中F-浓度为3×10-3 mol•L-1,再计算出钙离子的浓度;
(6)①阳极上氯离子失电子生成氯气,氯气和氢氧根离子反应生成次氯酸根离子和水,所以阳极反应式为Cl-+2OH--2e-═ClO-+H2O;
②Ni2+被ClO-氧化产生2NiOOH•H2O沉淀,其还原产物是氯离子.
解答 解:(1)Fe2O3和硫酸反应生成盐和水,反应方程式为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O,故答案为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(2)氧化钙和氧化钡与硫酸反应生成难溶的硫酸钙和硫酸钡,所以浸出渣主要成分为CaSO4•2H2O和BaSO4,故答案为:BaSO4;
(3)由于用氢氧化钠溶液调节溶液的pH值,容易引入杂质,所以方案是错误的;正确的操作应该是在调节pH前,应先在滤液中加入H2O2,使溶液中的Fe2+氧化为Fe3+,
故答案为:方案错误,在调节pH前,应先在滤液中加入H2O2,使溶液中的Fe2+氧化为Fe3+;
(4)由于CuS、S灼烧后溶于稀硫酸中生成硫酸铜,所以副产品应该是胆矾,即CuSO4•5H2O,
根据3Cu~2NO可知,0.1molCu反应生成NO为$\frac{0.2}{3}$mol,故3Cu2O~2NO反应生成NO为($\frac{2.24L}{22.4L/mol}$-$\frac{0.2}{3}$mol),可得混合物中Cu2O为(0.1mol-$\frac{0.2}{3}$mol)×$\frac{3}{2}$=0.05mol,故CuO为0.25mol-0.1mol-0.05mol=0.05mol,混合物中,0.1mol Cu不与稀H2SO4反应,0.05molCu2O、0.05molCuO与稀H2SO4反应,根据Cu2O、CuO中氧原子与H2SO4反应结合H+生成H2O,可得n(H2SO4)=0.05mol+0.05mol=0.1mol,
故答案为:CuSO4•5H2O;0.1;
(5)根据常温时CaF2的溶度积常数为2.7×10-11可知,溶液中F-浓度为3×10-3 mol•L-1,则Ca2+的浓度为$\frac{2.7×1{0}^{-11}}{(3×1{0}^{-3})^{2}}$=3×10-6 mol/L,所以则溶液中$\frac{c(C{a}^{2+})}{c({F}^{-})}$=$\frac{3×1{0}^{-6}}{3×1{0}^{-3}}$=1.0×10-3,故答案为:1.0×10-3;
(6)①阳极上氯离子失电子生成氯气,氯气和氢氧根离子反应生成次氯酸根离子和水,所以阳极反应式为Cl-+2OH--2e-═ClO-+H2O,故答案为:Cl-+2OH--2e-=ClO-+H2O;
②Ni2+被ClO-氧化产生2NiOOH•H2O沉淀,其还原产物是氯离子,则根据电子的得失守恒可知,反应的离子方程式为ClO-+2Ni2++4OH-=2NiOOH•H2O↓+Cl-,
故答案为:ClO-+2Ni2++4OH-=2NiOOH•H2O↓+Cl-.
点评 该题以废旧含镍催化剂生产NiO为载体,重点考查学生对工艺流程试题了解掌握情况,试题综合性强,贴近高考,侧重对学生能力的培养和训练,有利于培养学生的逻辑推理能力和规范严谨的实验设计能力以及动手操作能力;该类试题综合性强,理论和实践的联系紧密,有的还提供一些新的信息,这就要求学生必须认真、细致的审题,联系所学过的知识和技能,进行知识的类比、迁移、重组,全面细致的思考才能得出正确的结论.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将光亮的镁条放入盛有NH4Cl溶液的试管中 | 有大量气泡产生 | 反应中有NH3产生 |
| B | 向AgI悬浊液中滴加NaCl溶液 | 不出现白色沉淀 | 更难溶的物质无法转化为难溶的物质 |
| C | 向KI溶液中滴入少量氯水和苯,振荡、静置 | 溶液上层呈紫色 | I-还原性强于Cl- |
| D | 向某溶液中滴加氯水后再加入KSCN溶液 | 溶液呈红色 | 溶液中一定含有Fe2+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大气中PM2.5比表面积大,吸附力强,能吸附许多有毒有害物质 | |
| B. | 在厨房里可用米汤检验加碘食盐中的碘 | |
| C. | 14C可用于文物年代的鉴定,14C与12C互为同位素 | |
| D. | 喝补铁剂时,加服维生素C效果更好,原因是维生素C具有还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 自然界存在丰富的碳、氮、硅、磷、铁等元素,它们可形成单质及许多化合物.按要求回答下列问题:
自然界存在丰富的碳、氮、硅、磷、铁等元素,它们可形成单质及许多化合物.按要求回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
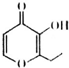 俗称“一滴香”的物质被人食用后会损伤肝脏,还能致癌.“一滴香”的分子结构如图所示,下列说法正确的是( )
俗称“一滴香”的物质被人食用后会损伤肝脏,还能致癌.“一滴香”的分子结构如图所示,下列说法正确的是( )| A. | 该有机物的分子式为C8H8O3 | |
| B. | 1 mo1该有机物最多能与 2 mol H2发生加成反应 | |
| C. | 该有机物能发生取代、加成和氧化反应 | |
| D. | 该有机物能与碳酸氢钠反应生成CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

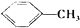 $→_{△}^{MnO_{4}/H+}$
$→_{△}^{MnO_{4}/H+}$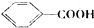
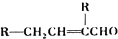
 .
. .
. (写出其中一种结构简式)
(写出其中一种结构简式) .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
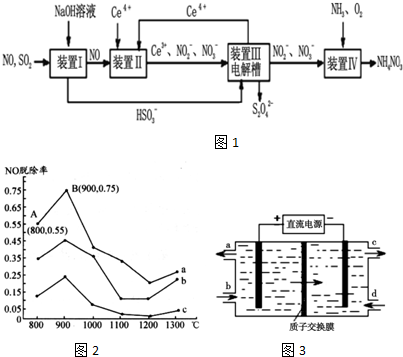
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


 ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com