
| A. | 在pH=1的无色溶液中:SO42-、Cu2+、Na+、Cl- | |
| B. | 使pH试纸呈红色的溶液中:Fe2+、NO3-、SO42-、Na+ | |
| C. | 加入铝粉后产生大量氢气的溶液中:NH4+、Na+、NO3-、SO42- | |
| D. | 在$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×1013的溶液中:NH4+、Ca2+、C1-、K+ |
分析 A.Cu2+为蓝色;
B.使pH试纸呈红色的溶液,显酸性;
C.加入铝粉后产生大量氢气的溶液,为非氧化性酸或强碱溶液;
D.在$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×1013的溶液,显酸性.
解答 解:A.Cu2+为蓝色,与无色溶液不符,故A错误;
B.使pH试纸呈红色的溶液,显酸性,Fe2+、NO3-、H+发生氧化还原反应,不能大量共存,故B错误;
C.加入铝粉后产生大量氢气的溶液,为非氧化性酸或强碱溶液,酸性溶液中Al、NO3-发生氧化还原反应不生成氢气,碱性溶液中不能大量存在NH4+,故C错误;
D.在$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×1013的溶液,显酸性,该组离子之间不反应,可大量共存,故D正确;
故选D.
点评 本题考查离子共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2mol/L NaCl溶液中含有Na+个数为2NA | |
| B. | 常温常压下,80g NH4NO3中含有氮原子数是NA | |
| C. | 18gNH4+中含有的电子数为10NA | |
| D. | 5.6g铁与稀硝酸反应转移的电子数目一定为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加N2的浓度能加快反应速率 | |
| B. | 降低体系温度能加快反应速率 | |
| C. | 使用催化剂不影响反应速率 | |
| D. | 若反应在密闭容器中进行,N2和H2能100%转化为NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 34S原子核内中子数为16 | B. | 1H218O的摩尔质量为20g/mol | ||
| C. | 13C和15N原子核内的质子数相差2 | D. | 2H+的核外电子数为2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正丁烷分子储存的能量大于异丁烷分子 | |
| B. | 正丁烷的稳定性大于异丁烷 | |
| C. | 异丁烷转化为正丁烷的过程是一个放热过程 | |
| D. | 异丁烷分子中的碳氢键比正丁烷的多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
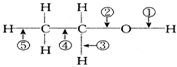
| A. | 和金属钠作用时,键①断裂 | |
| B. | 和浓H2SO4共热至170℃时,键②和⑤断裂 | |
| C. | 在Ag催化剂下和O2反应时,键①和③断裂 | |
| D. | 和CH2COOH共热时,键②断裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MnO2 | B. | 稀盐酸 | C. | Na2SO3溶液 | D. | KMnO4溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com