
【题目】乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平。请回答下列问题。
(1)乙烯的电子式____________,结构简式____________。
(2)鉴别甲烷和乙烯的试剂是______(填序号)。
A.稀硫酸 B.溴的四氯化碳溶液
C.水 D.酸性高锰酸钾溶液
(3)下列物质中,可以通过乙烯加成反应得到的是______(填序号)。
A.CH3CH3 B.CH3CHCl2
C.CH3CH2OH D.CH3CH2Br
(4)已知 2CH3CHO+O2![]() 2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如下图所示。
2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如下图所示。
![]()
反应②的化学方程式为____________________________________。 工业上以乙烯为原料可以生产一种重要的合成有机高分子化合物,其反应的化学方程式为____________________________________。
【答案】![]() H2C=CH2 BD ACD 2CH3CH2OH+O2
H2C=CH2 BD ACD 2CH3CH2OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O ![]()
【解析】
(1)乙烯中含有碳碳双键,据此分析解答;
(2)乙烯中含有碳碳双键,可以发生加成反应,可以被强氧化剂氧化,而甲烷不能;
(3)乙烯加成反应的特征是原子或原子团加在双键碳原子上,双键变为单键;
(4)乙烯可以和水加成生成乙醇,乙醇可以被氧化为乙醛,乙醛继续被氧化为乙酸;乙烯可以发生加聚反应生成聚乙烯。
(1)乙烯中含碳碳双键,电子式为:![]() ,根据电子式可以书写结构简式为H2C=CH2,故答案为:
,根据电子式可以书写结构简式为H2C=CH2,故答案为:![]() ;H2C=CH2;
;H2C=CH2;
(2)乙烯中含有碳碳双键,可以发生加成反应,使溴水褪色,可以被强氧化剂高锰酸钾氧化,从而使高锰酸钾褪色,而甲烷不能,故答案为:BD;
(3)乙烯和溴化氢发生加成生成溴乙烷,和水加成生成乙醇,和氢气加成生成乙烷,与氯气加成生成1,2-二溴乙烷,得不到CH3CHCl2,故答案为:ACD;
(4)乙烯可以和水加成生成乙醇,所以A是乙醇,乙醇可以被氧化为B乙醛,乙醛继续被氧化为乙酸,乙醇的催化氧化反应为:2CH3CH2OH+O2![]() 2CH3CHO+2H2O;乙烯可以发生加聚反应生成聚乙烯,反应为:
2CH3CHO+2H2O;乙烯可以发生加聚反应生成聚乙烯,反应为:![]() ,故答案为:2CH3CH2OH+O2
,故答案为:2CH3CH2OH+O2![]() 2CH3CHO+2H2O;
2CH3CHO+2H2O;![]() 。
。


科目:高中化学 来源: 题型:
【题目】Ⅰ.重铬酸钾(K2Cr2O7)是一种强氧化剂,在实验室和工业中都有很广泛的应用。同时,由于其具有致癌作用,也是环境污染物之一,必须进行处理。工业上通常以铬铁矿(主要成分为FeO·Cr2O3,另外还含有SiO2、Al2O3等杂质)为原料制备重铬酸钾,主要流程如下图所示:
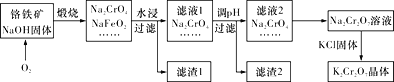
已知:①NaFeO2遇水强烈水解,生成红褐色物质;
②2CrO42- (黄色)+2H+![]() Cr2O72- (橙色)+H2O。
Cr2O72- (橙色)+H2O。
请回答下列问题:
(1)滤液1的溶质除Na2CrO4、Na2SiO3外,还含有________________(填化学式);
(2)由滤液2转化为Na2Cr2O7溶液过程中,能说明反应达平衡状态的是________(填字母代号);
a.溶液的颜色不变
b.v(CrO![]() )=2v(Cr2O
)=2v(Cr2O![]() )
)
c.Cr2O![]() 和CrO
和CrO![]() 的浓度相同
的浓度相同
(3)向Na2Cr2O7溶液中加入KCl固体,获得K2Cr2O7晶体的操作依次是加热浓缩、______________、过滤、洗涤、干燥。
Ⅱ.工业废水中常含有一定量的Cr2O![]() 和CrO
和CrO![]() ,常用还原沉淀法处理。该方法的工艺流程为:
,常用还原沉淀法处理。该方法的工艺流程为:
CrO![]()
![]() Cr2O
Cr2O![]()
![]() Cr3+
Cr3+![]() Cr(OH)3
Cr(OH)3
(4)请写出Cr2O![]() 与FeSO4溶液在酸性条件下反应的离子方程式:______________________。
与FeSO4溶液在酸性条件下反应的离子方程式:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z为元素周期表中原子序数依次增大的三种短周期元素,Y与X、Z均相邻,X、Y与Z三种元素原子的最外层电子数之和为19;W的单质为生活中一种常见的金属,在Z元素的单质中燃烧产生棕黄色的烟,生成![]() 。回答下列问题:
。回答下列问题:
(1)Z元素在元素周期表中的第____周期。
(2)![]() 与足量的
与足量的![]() 的水溶液发生反应生成两种强酸,写出该反应的离子方程式____。
的水溶液发生反应生成两种强酸,写出该反应的离子方程式____。
(3)![]() 易升华,易溶于水,乙醇/丙酮等溶剂。据此推测其晶体熔化时克服的作用力是__,判断的依据是____。
易升华,易溶于水,乙醇/丙酮等溶剂。据此推测其晶体熔化时克服的作用力是__,判断的依据是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)实验室用金属铜和稀硝酸制取NO的离子方程式为______________________。
(2)NO是有毒气体,某学生为防止污染,用分液漏斗和烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图甲所示。
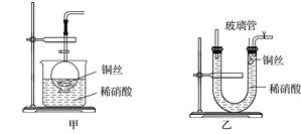
①实验室若没有铜丝,而只有小铜粒,在使用上述装置进行实验时,可用丝状材料包裹铜粒以代替铜丝进行实验,这种丝状材料的成分可以是________(填序号)。
A.铁 B.铝 C.铂 D.玻璃
②打开分液漏斗的活塞使反应进行,在分液漏斗中实际看到的气体是红棕色的,原因是__________(填化学方程式)。
(3)为证明铜丝与稀硝酸反应生成的确实是NO,某学生另设计了一套如图乙所示的装置制取NO。反应开始后,可以在U形管右端观察到无色的NO气体。
①长玻璃管的作用是______________________________________________________。
②让反应停止的操作方法及原因是__________________________________________。
(4)以下收集NO气体的装置,合理的是________(填序号)。
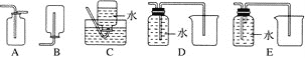
(5)将32.64 g铜与140 mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2 L。请回答:
①NO的体积为________ L,NO2的体积为________ L。
②待产生的气体全部释放后,向溶液中加入VmLamol·L-1的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为________ mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.28g N2含有的原子数为NA
B.1mol Zn与足量盐酸反应失去的电子数为2NA
C.标准状况下22.4L水中含有的H2O分子数为NA
D.2mol /L NaCl溶液中含有Na+个数为2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别按下图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中A为电流表。请回答下列问题:
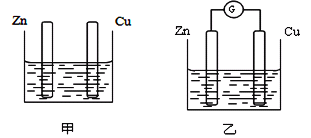
(1)以下叙述中,正确的是________(填字母)。
A.甲中锌片是负极,乙中铜片是正极
B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液pH均增大
D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向Zn→Cu
F.乙溶液中SO42-向铜片方向移动
(2)变化过程中能量转化的主要形式:甲为________;乙为____________。
(3)在乙实验中,某同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是_______________________ 。
(4)在乙实验中,如果把硫酸换成硫酸铜溶液,请写出铜电极的电极反应式__________________。当电路中转移0.2 mol电子时,消耗负极材料的质量为_________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室验证钠能与二氧化碳发生反应,并确定其产物的装置如图所示(已知:![]() 溶液遇
溶液遇![]() 能产生黑色的
能产生黑色的![]() ),下列说法错误的是( )
),下列说法错误的是( )
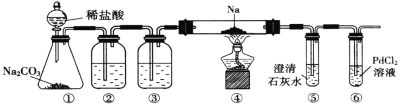
A.装置①的仪器还可以制取![]() 、
、![]() 等气体
等气体
B.装置⑤中石灰水变浑浊后,再点燃酒精灯
C.装置②③中分别盛装饱和![]() 溶液、浓
溶液、浓![]()
D.装置⑥中有黑色沉淀,发生的反应是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水的离子积常数Kw与温度T(℃)的关系如图D3-5所示:
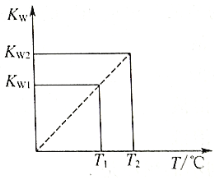
(1)若T1=25℃,则Kw1=_____________;若T2=100℃时,Kw2=10-12,则此时0.05mol/L的Ba(OH)2溶液的pH=_____________。
(2)已知25℃时,0.1L 0.1mol/L的NaA溶液的pH=10,则NaA溶液中存在的平衡有_______________________________________________。
溶液中各离子的物质的量浓度由大到小的顺序为__________________________。
(3)25℃时,将pH=11的NaOH溶液与pH=4的硫酸溶液混合,若所得混合溶液的pH=9,则NaOH溶液与硫酸溶液的体积比为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是重要的化工原料,以乙烯为原料在不同条件下可合成下列物质(部分条件未标出):

按下列要求写出:
(1)聚乙烯的结构简式是_____________,乙醛的结构简式是_____________;
(2)反应①的化学方程式是________________________________,反应类型是___________;
(3)反应③的化学方程式是________________________________,反应类型是___________;
(4)反应⑤的化学方程式是________________________________,反应类型是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com