
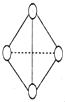
 ����A��B��C��D��E��F���ֶ���������Ԫ�أ����ǵ�ԭ��������������D��Eͬ���壬��D���⻯�ﳣ��ʱΪҺ̬��A��B������������֮����C��������������ȣ�A�ֱ���B��C��D�γɵ���������ȵķ��ӣ�
����A��B��C��D��E��F���ֶ���������Ԫ�أ����ǵ�ԭ��������������D��Eͬ���壬��D���⻯�ﳣ��ʱΪҺ̬��A��B������������֮����C��������������ȣ�A�ֱ���B��C��D�γɵ���������ȵķ��ӣ�


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
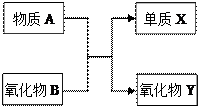 A��B��X��Y��Ϊ��ѧ�εij������ʣ�����֮���ת����ϵ��ͼ��ʾ����д���������������Ļ�ѧ����ʽ��
A��B��X��Y��Ϊ��ѧ�εij������ʣ�����֮���ת����ϵ��ͼ��ʾ����д���������������Ļ�ѧ����ʽ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ˮ�����c��H+��=10-12mol?L-1����Һ�У�Cl-��CO32-��K+��SO32- |
| B�����д���AlO2-����Һ�У�K+��Al3+��Br-��HCO3- |
| C��1.0mol?L-1��KNO3��Һ��H+��Fe2+��Cl-��SO42- |
| D��ʹpH��ֽ������ɫ����Һ�У�Cl-��K+��Mg2+��SO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��һ�� | �ڶ��� | ������ | |
| ��Ʒ������/g | 7.540 | 15.08 | 35.00 |
| ������������/L | 0.6720 | 1.344 | 2.688 |
| �������/g | 0.8000 | 1.600 | 3.200 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������Һ�������ǣ������� |
| B���Ҵ������ᣩ����KOH��Һ����Һ |
| C���״���Һ�����ᣩ����NaOH��Һ������ |
| D������Һ�����ͣ�����ʳ�ν��衢���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Һʱ����Һ©�����²�Һ����¿ڷų����ϲ�Һ����Ͽڵ��� |
| B������ʱ����ȴˮӦ���������¶˽��� |
| C������ʱ��Ҫ�ò��������Ͻ�����Һ |
| D������ʱ���������˵�Һ��ֱ�ӵ���©����ʹҺ�������ֽ�ı�Ե |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com