
分析 在水溶液里或熔融状态下能够完全电离的化合物是强电解质;
在水溶液里或熔融状态下能部分电离的化合物是强电解质;
在水溶液里和熔融状态下都不导电的化合物是非电解质;
含有自由移动电子或离子的物质能导电;
一水合氨为弱电解质,部分电离;
硝酸钾为强电解质,完全电离.
解答 解:(1)Cu是单质,含有自由电子,能够导电;既不是电解质,也不是非电解质;
(2)烧碱固体,不含自由移动电子或离子,不能导电;在水溶液里或熔融状态下能够完全电离的化合物是强电解质;
(3)氯气不含自由移动电子或离子,不能导电;是单质,既不是电解质,也不是非电解质;
(4)碳酸钠粉末,不含自由移动电子或离子,不能导电;在水溶液里或熔融状态下能够完全电离的化合物是强电解质;
(5)稀硫酸,含有自由离子,能够导电;属于混合物,既不是电解质,也不是非电解质;
(6)NH3.H2O不含自由移动电子或离子,不能导电;在水溶液里能部分电离,属于弱电解质;
(7)硫酸钠溶液,含有自由离子,能够导电;属于混合物,既不是电解质,也不是非电解质;
(8)乙醇不含自由移动电子或离子,不能导电;在水溶液里和熔融状态下都不导电的化合物是非电解质;
(9)熔融的硝酸钾,含有自由离子,能导电;在水溶液里或熔融状态下能够完全电离的化合物是强电解质;
①其中能导电的是(1)(5)(7)(9);
属于强电解质的是(2)(4)(9);
属于弱电解质的是(6);
故答案为:(1)(5)(7)(9);(2)(4)(9);(6);
②一水合氨为弱电解质,部分电离,电离方程式:NH3•H2O?NH4++OH-,
故答案为:NH3•H2O?NH4++OH-;
硝酸钾为强电解质,完全电离,电离方程式:KNO3=K++NO3-;
故答案为:KNO3=K++NO3-.
点评 本题考查了电解质、非电解质,强电解质、弱电解质的判断,电解质电离方程式的书写,明确概念是解题关键,注意单质、混合物既不是电解质、也不是非电解质,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:多选题
| A. | 向水中加入少量硫酸氢钠固体 | B. | 向水中加入少量硫酸铝固体 | ||
| C. | 向水中加入少量氯化铵固体 | D. | 将水加热到100℃,使水的pH=6 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

| V(AgNO3)/mL | 15.00 | 19.00 | 19.80 | 19.98 | 20.00 | 20.02 | 21.00 | 23.00 | 25.00 |
| E/mV | -225 | -200 | -150 | -100 | 50.0 | 175 | 275 | 300 | 325 |
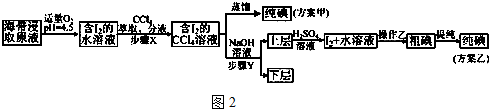
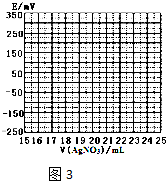
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑ | B. | 4Fe(OH)2+O2+2H2O=4Fe(OH)3 | ||
| C. | 2F2+2H2O=4HF+O2↑ | D. | 2Na+2H2O=2NaOH+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| Ca2+ | Mg2+ | Fe3+ | |
| 开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
| 完全沉淀时的pH | 13.9 | 11.1 | 3.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用分液漏斗和烧杯分离水和乙酸乙酯的混合物 | |
| B. | 用瓷坩埚熔融烧碱 | |
| C. | 用玻璃棒蘸少量待测物质的浓溶液做焰色反应 | |
| D. | 将pH试纸直接插入溶液中测量某溶液pH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 150mL 1 mol/L的NaCl溶液 | B. | 75mL 2 mol/L的NH4Cl溶液 | ||
| C. | 150mL 3 mol/L的KCl溶液 | D. | 75mL 1 mol/L的BaCl2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ||||||||
| 二 | A | B | C | |||||
| 三 | D | E | F | G |
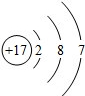 .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com