
【题目】A为两种金属组成的合金,发生如图所示的变化: 
(1)合金A由和组成;
(2)写出下列变化的离子方程式: C→E;
D→F .
【答案】
(1)Fe;Al
(2)Al3++4OH﹣═AlO2﹣+2H2O;Fe(OH)3+3H+=Fe3++3H2O
【解析】解:含Fe2+溶液是浅绿色的,能被氯气氧化为Fe3+ , Al可以和盐酸反应得到可溶性的含有Al3+的盐,铝离子和过量的NaOH反应会生成偏铝酸钠的水溶液,向其中加盐酸会出现氢氧化铝沉淀, 所以合金是金属铁和铝的合金,B是氯化亚铁溶液,C是氯化铁溶液,D是氢氧化铁沉淀,E是偏铝酸钠溶液,G是氢氧化铝.(1)合金是金属铁和铝的合金,所以答案是:Fe;Al;(2)氯化铝和过量的氢氧化钠反应的离子方程式为:Al3++4OH﹣═AlO2﹣+2H2O,氢氧化铁溶于盐酸的离子方程式为:Fe(OH)3+3H+=Fe3++3H2O,
所以答案是:Al3++4OH﹣═AlO2﹣+2H2O,Fe(OH)3+3H+=Fe3++3H2O.


科目:高中化学 来源: 题型:
【题目】单晶硅是信息产业中重要的基础材料。通常用焦炭在高温下还原二氧化硅制得粗硅(含铁、铝、硼、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度450~500℃),四氯化硅经提纯后用氢气还原可得高纯硅。以下是实验室制备四氯化硅的装置示意图。
相关信息如下:
a.四氯化硅遇水极易水解;
b.硼、铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
c.有关物质的物理常数见下表:
物 质 | SiCl4 | BCl3 | AlCl3 | FeCl3 | PCl5 |
沸点/℃ | 57.7 | 12.8 | - | 315 | - |
熔点/℃ | -70.0 | -107.2 | - | - | - |
升华温度/℃ | - | - | 180 | 300 | 162 |
请回答下列问题:
(1)写出装置A中发生反应的离子方程式。
(2)装置A中g管的作用是;装置C中的试剂是;装置E中的h瓶需要冷却的理由是。
(3)装置E中h瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后的残留物中,除铁元素外可能还含有的杂质元素是(填写元素符号)。
(4)为了分析残留物中铁元素的含量,先将残留物预处理,使铁元素还原成
Fe2+ , 再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O
①滴定前是否要滴加指示剂?(填“是”或“否”),请说明理由。
②某同学称取5.000g残留物,经预处理后在容量瓶中配制成100mL溶液,移取25.00mL试样溶液,用1.000×10-2mol·L-1KMnO4标准溶液滴定。达到滴定终点时,消耗标准溶液20.00mL,则残留物中铁元素的质量分数是。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,50mL pH=1的稀H2SO4和盐酸的混合液与50mL Ba(OH)2溶液相混合,充分反应后过滤,得0.466g沉淀,滤液的pH值变为13.求:
(1)原混合液中SO42﹣ 和Cl﹣的物质的量;
(2)Ba(OH)2溶液的物质的量浓度.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】太阳能电池的发展已经进入了第三代。第一代为单晶硅太阳能电池,第二代为多晶硅、非晶硅等太阳能电池,第三代就是铜铟镓硒CIGS(CIS中掺入Ga)等化合物薄膜太阳能电池以及薄膜Si系太阳能电池。亚铜离子(Cu+)基态时的价电子排布式表示为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.95℃纯水的pH<7,说明加热可导致水呈酸性
B.25℃时,在纯水中加入强碱溶液不会影响水的离子积常数
C.pH=3的醋酸溶液加水稀释10倍后pH=4
D.pH=3和pH=5的盐酸各10mL混合所得溶液的pH=4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属铬和氢气在工业上都有重要的用途.已知:铬能与稀硫酸反应,生成氢气和硫酸亚铬(CrSO4).铜铬构成原电池如图所示,盐桥中装的是饱和KCl琼脂溶液,下列关于此电池的说法正确的是( ) 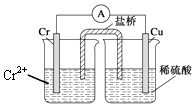
A.盐桥的作用是使整个装置构成通路、保持溶液呈电中性,凡是有盐桥的原电池,盐桥中均可以用饱和KCl琼脂溶液
B.理论上1molCr溶解,盐桥中将有2molCl﹣进入左池,2molK+进入右池
C.此过程中H+得电子,发生氧化反应
D.电子从铬极通过导线到铜极,又通过盐桥到转移到左烧杯中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】采用脱硫技术可以把煤炭燃烧过程中的硫元素以CaSO4的形式固定,从而降低SO2的排放.相关反应的热化学方程式如下: CaSO4(s)+CO(g)CaO(s)+SO2(g)+CO2(g)△H1=+218.4kJmol﹣1(反应Ⅰ)
CaSO4(s)+4CO(g)CaS(s)+4CO2(g)△H2=﹣175.6kJmol﹣1(反应Ⅱ)
假设某温度下,反应Ⅰ的速率(v1)大于反应Ⅱ的速率(v2),则下列反应过程能量变化示意图正确的是( )
A.
B.
C.
D.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物甲(由氮和另一种常见的主族元素组成)是一种新型无机材料.将8.2g甲溶于足量的氢氧化钠溶液,可产生标准状况下为4.48L的气体,该气体可作制冷剂.向反应后的溶液中逐滴加入稀盐酸,产生白色沉淀质量最大为15.6g,继续滴加沉淀消失.则甲溶于氢氧化钠的化学方程式为
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com