
【题目】分子式为C3H7Br 的有机物甲在适宜的条件下能发生如下一系列转化:
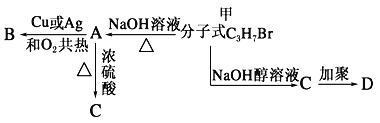
(1)若B能发生银镜反应,试回答下列问题:
①试确定有机物甲的结构简式:___________;
②用化学方程式表示下列转化过程:甲+ NaOH:___________________B+Ag(NH3)2OH:_________________
(2)若B不能发生银镜反应,请回答下列问题:
①试确定A的结构简式______________;
②用化学方程式表示下列转化过程:甲+NaOH![]() ____________________A→B:_____________________C→D:_____________________
____________________A→B:_____________________C→D:_____________________
【答案】CH3CH2CH2Br CH3CH2CH2Br+NaOH![]() CH3CH2CH2OH+NaBr CH3CH2CHO+2Ag(NH3)2OH
CH3CH2CH2OH+NaBr CH3CH2CHO+2Ag(NH3)2OH![]() CH3CH2COONH4+3NH3+2Ag↓+H2O CH3CHOHCH3 CH3CHBrCH3+NaOH
CH3CH2COONH4+3NH3+2Ag↓+H2O CH3CHOHCH3 CH3CHBrCH3+NaOH![]() CH3CH=CH2↑+NaBr+H2O 2CH3CHOHCH3+O2
CH3CH=CH2↑+NaBr+H2O 2CH3CHOHCH3+O2![]() 2
2![]() +2H2O nCH3CH=CH2
+2H2O nCH3CH=CH2![]()
![]()
【解析】
(1)若B能发生银镜反应,则说明甲的水解产物A中-OH所在的碳原子上有2个氢原子,则A为1-丙醇,即甲为1-溴丙烷,B为丙醛,C为1-丙醇的消去产物,为丙烯,D为聚丙烯;
(2)若B不能发生银镜反应,则甲为CH3CHBrCH3,A为CH3CH(OH)CH3,B为![]() ,以此来解答。
,以此来解答。
(1)若B能发生银镜反应,则说明甲的水解产物A中-OH所在的碳原子上有2个氢原子,则A为1-丙醇,即甲为1-溴丙烷,B为丙醛,C为1-丙醇的消去产物,为丙烯,D为聚丙烯;
①由以上分析可知甲为1-溴丙烷,为CH3CH2CH2Br;
②甲转化为A,是1-溴丙烷发生卤代烃的水解反应,故化学方程式为CH3CH2CH2Br+NaOH![]() CH3CH2CH2OH+NaBr;B为丙醛,能和银氨溶液Ag(NH3)2OH发生银镜反应,化学方程式为CH3CH2CHO+2Ag(NH3)2OH
CH3CH2CH2OH+NaBr;B为丙醛,能和银氨溶液Ag(NH3)2OH发生银镜反应,化学方程式为CH3CH2CHO+2Ag(NH3)2OH![]() CH3CH2COONH4+3NH3+2Ag↓ +H2O;
CH3CH2COONH4+3NH3+2Ag↓ +H2O;
(2)若B不能发生银镜反应,则甲为CH3CHBrCH3,A为CH3CH(OH)CH3,B为![]() ;
;
①由上述分析可知,A的结构简式为CH3CH(OH)CH3;②甲+NaOH![]() 的反应为CH3CHBrCH3+NaOH
的反应为CH3CHBrCH3+NaOH![]() CH3CH=CH2↑+NaBr+H2O;反应类型为消去反应;A→B的反应为2CH3CH(OH)CH3+O2
CH3CH=CH2↑+NaBr+H2O;反应类型为消去反应;A→B的反应为2CH3CH(OH)CH3+O2![]() 2
2![]() +2H2O;C→D的反应为nCH3CH=CH2
+2H2O;C→D的反应为nCH3CH=CH2![]()
![]() 。
。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】四种常见元素的性质或结构信息如F表所示,请问答下列问题。
元素 | A | B | R | D |
相关信息 | 基态原子核外电子占据3个能级且最高能级上有3个电子 | B的单质是最常见半导体材料 | 位于第四周期IB族 | 是非金属元素,其形成的某种单质是电的良导体,有的分子形状似足球 |
(1)R的基态原子价层电子排布式为________,这四种元素的第一电离能由大到小的顺序为________________(写元素符号)。
(2)A、B,D均可形成多种氢化物,在最常见的三种氢化物中,分子构型为三角锥的氢化物分子式为_______,任意写出一种中心原子存在sp2、sp3两种杂化类型的物质的结构简式________,与A的常见单质互为等电子体的上述元素的氧化物是________。
(3)B、D均可形成氧化物,等物质的量的B、D的最高价氧化物中σ键之比为________,已知有下列两种数据:
键能(kJ/mol) | 熔点(K) | 沸点(K)) | |
BO2 | B-O:452 | 1923 | 2503 |
DO2 | D=O:615,D-O:348 | 216 | 195 |
请解释键能大小与两种氧化物熔点、沸点高低差异过大的原因________。
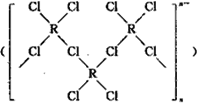
(4)在一定条件下,Cl-与R2+可形成一种无限长链离子,研究表明该离子中每个氯原子最外层均达到8电子稳定结构,有些氧与R之间存在配位键,若该长链离子中含有n个R,则该离子的化学式为________。
(5)A元素能形成组成为Pt(AH3)2Cl2的配合物,该配合物存在两种同分异构体:一种为淡黄色(Q),不具有抗癌作用,在水中的溶解度小;另一种为黄绿色(P),具有抗癌作用,在水中的溶解度较大。
①Q是________(填“极性”或“非极性”)分子,
②P的结构简式为________(AH3配体作为一个整体写)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液X,由Na+、Ag+、Ba2+、Al3+、Fe3+、AlO2﹣、CO32﹣、SO42﹣中的若干种离子组成,取该溶液进行如下实验:
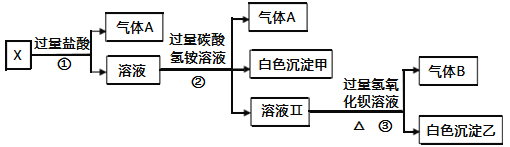
(1)气体A的成分是________(填化学式,下同),气体B的成分是________。
(2)写出步骤①发生反应的所有离子方程式________________________。
(3)写出步骤②形成白色沉淀甲的离子方程式________________________。
(4)通过上述实验,可确定X溶液中一定存在的离子是________,尚未确定是否存在的离子是________,只要设计一个简单的后续实验就可以确定该离子是否存在,该方法是________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第三周期元素,浓度均为0.01mol/L的最高价氧化物对应水化物的pH与原子半径的关系如图所示。则下列说法正确的是( )

A.气态氢化物的稳定性:N>R
B.Z的最高价氧化物对应的水化物能溶于稀氨水
C.Y和R形成的化合物既含离子键又含共价键
D.X和M两者最高价氧化物对应的水化物反应后溶液的pH>7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案能达到实验目的的是( )
A | B | C | D | |
实验方案 |
置于光亮处 |
片刻后在Fe电极附近滴入K3[Fe(CN)6]溶液 |
|
|
实验目的 | 验证甲烷与氯气发生化学反应 | 验证Fe电极被保护 | 验证乙炔的还原性 | 验证铁钉发生析氢腐蚀 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaCl是我们生活中必不可少的物质。将NaCl固体溶于水,溶解过程如图所示,下列说法正确的是
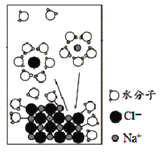
A.该过程发生了分解反应
B.离子从固体表面脱离后不会再回到固体表面
C.水合Na+的图示不科学
D.NaCl溶于水后发生了电离,是在通电条件下进行的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于离子的检验说法正确的是
A.向某溶液中滴入足量盐酸,如观察到无色无味的气体产生,且能使澄清石灰水变浑浊,即证明溶液中必定有![]()
B.向某无色溶液中加入BaCl2溶液,有白色沉淀出现,再加入稀盐酸,沉淀不消失,无法证明溶液一定含有![]()
C.向某无色溶液中加入少量稀氢氧化钠溶液后,用湿润的红色石蕊试纸靠近试管口,若试纸不变蓝,则说明该溶液中无![]()
D.如透过蓝色的钴玻璃能够观察到紫色火焰,则一定有钾元素,一定不含有钠元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用氯氧化法处理含氰(CN-)废水,一定条件下,氯气和CN-反应生成无毒气体N2和CO2。下列说法不正确的是( )
A.CN-中碳元素的化合价为+2B.该反应的氧化产物是N2
C.反应中氧化剂和还原剂的系数比为5:2D.该反应的还原产物为Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示一些晶体中的某些结构,它们分别是NaCl、CsCl、干冰、金刚石、石墨晶体结构中的某一种的某一部分。
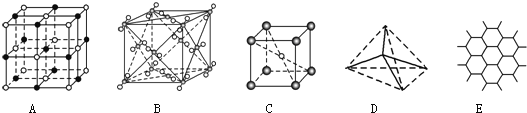
(1)代表金刚石的是________(填字母编号,下同),其中每个碳原子与______个碳原子最近且距离相等;金刚石属于________晶体。
(2)代表石墨的是_______,每个正六边形占有的碳原子数平均为_______个;
(3)代表NaCl的是_______,每个Na+周围与它最近且距离相等的Na+有_______个;
(4)代表CsCl的是_______,它属于_______晶体,每个Cs+与个_______Cl-紧邻;
(5)代表干冰的是_______,它属于_______晶体,每个CO2分子与_______个CO2分子紧邻;
(6)则上述五种物质熔点由高到低的排列顺序为______________(用字母编号回答)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com