
| A、碳酸钾 | B、硫酸钠 |
| C、碳酸钠 | D、硫酸钾 |


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
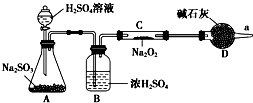 ①某学生根据SO2具有还原性判断SO2和Na2O2反应能生成硫酸钠,该同学无法断定反应中是否有氧气生成,拟使用如图所示装置进行实验(A为SO2的发生装置,图中铁架台等装置已略去).
①某学生根据SO2具有还原性判断SO2和Na2O2反应能生成硫酸钠,该同学无法断定反应中是否有氧气生成,拟使用如图所示装置进行实验(A为SO2的发生装置,图中铁架台等装置已略去).查看答案和解析>>
科目:高中化学 来源: 题型:
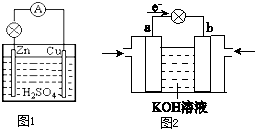 原电池是直接把化学能转化为电能的装置.
原电池是直接把化学能转化为电能的装置.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②③⑥ | B、②③④ |
| C、④⑤⑥ | D、①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2的热值(单位质量的燃料完全燃烧时所放出的热量,叫做燃料的热值)为142.9kJ?g-1,则氢气燃烧的热化学方程式可表示为:2H2(g)+O2(g)=2H2O(l)△H=-285.8kJ?mol-1 |
| B、反应A(g)═2B(g),若正反应的活化能为Ea kJ?mol-1,逆反应的活化能为Eb kJ?mol-1,则△H=(Ea-Eb)kJ?mol-1 |
| C、能自发进行的化学反应,一定是△H<0、△S>0 |
| D、增大反应物浓度,可增大单位体积内活化分子百分数,从而增加有效碰撞的次数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com