
【题目】某有机物0.1摩和标准状况下的氧气5.6升恰好反应完全,所得产物为CO2、CO、H2O(气),产物通过盛浓硫酸的洗气瓶,洗气瓶的质量增加了5.4克,再通过足量灼热的氧化铜,氧化铜的质量减轻了1.6克,再通过装有碱石灰的干燥管,干燥管增加了8.8克。
(1)求有机物的分子式,
(2)若此有机物能与钠反应,写出其结构简式。
【答案】计算过程(3分)分子式C2H6O(1分)结构简式CH3CH2OH或 C2H5OH(1分)
【解析】试题分析:(1)通过洗气瓶增重求出水的质量为5.4g,物质的量是5.4g÷18g/mol=0.3mol;氧化铜减轻1.6g,根据方程式CuO+CO![]() CO2+Cu可知氧化铜的物质的量是1.6g÷16g/mol=0.1mol,所以参加反应的CO质量为2.8g,物质的量是0.1mol,同时生成CO2是4.4g;碱石灰增重8.8g,因此有机物燃烧生成的CO2的质量为8.8g-4.4g=4.4g。根据质量守恒定律可知有机物的质量是5.4g+2.8g+4.4g-
CO2+Cu可知氧化铜的物质的量是1.6g÷16g/mol=0.1mol,所以参加反应的CO质量为2.8g,物质的量是0.1mol,同时生成CO2是4.4g;碱石灰增重8.8g,因此有机物燃烧生成的CO2的质量为8.8g-4.4g=4.4g。根据质量守恒定律可知有机物的质量是5.4g+2.8g+4.4g-![]() =4.6g,所以该有机物的物质的相对分子质量=4.6÷0.1=46。有机物碳、氢、氧比为C:H:O=0.2:0.6:0.1=2:6:1,所以它的分子式为C2H6O;
=4.6g,所以该有机物的物质的相对分子质量=4.6÷0.1=46。有机物碳、氢、氧比为C:H:O=0.2:0.6:0.1=2:6:1,所以它的分子式为C2H6O;
(2)此有机物能与钠反应,这说明分子中含有羟基,其结构简式为CH3CH2OH或 C2H5OH。


 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:
【题目】现有部分元素的性质与原子(或分子)结构如下表所示:
元素编号 | 元素性质与原子(或分子)结构 |
T | 最外层电子数是次外层电子数的3倍 |
X | 常温下单质分子为双原子分子,分子中含有3对共用电子对 |
Y | M层比K层少1个电子 |
Z | 第三周期元素的金属离子中半径最小 |
U | 第三周期元素的非金属离子还原性最弱 |
(1)写出元素T含有10个中子的原子符号:_________________。写出X与Y形成的化合物的电子式______________。
(2)Y与Z相比,金属性较强的是________(填元素符号),下列表能证明这一事实的是__________(填字母)。
a.Y单质的熔点比Z单质低 b.Y单质与水反应比Z单质与水反应剧烈
c.Y的化合价比Z低 d.Y最高价氧化物对应的水化物的碱性比Z的强
(3)写出Z与U最高价氧化物对应的水合物相互反应的方程式____________________________
(4)M物质由T、Y、Z三种元素组成,请写出含0.1 mol的M溶液与60mL5 mol·L-1
的盐酸反应的离子反应式________________________________
(5)元素X与氢元素以原子个数比1∶2化合形成常用于火箭燃料的化合物元素T和氢元素以原子个数比为1∶1化合形成化合物Q,Q与W发生氧化还原反应,反应的产物不污染环境,写出该反应的化学方程式:__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 凡是放热反应都是自发的,吸热反应都是非自发的
B. 自发反应的熵一定增大,非自发反应的熵一定减小或不变
C. ΔH<0、ΔS<0的反应一定能自发进行
D. ΔH>0、ΔS<0的反应一定不能自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各种微粒在水溶液中能大量共存的是
A. Ba2+、Na+、CO32-、NO3- B. H+、K+、I-、ClO-
C. Fe2+、Al+、NO3-、HCO- D. Cu2+、Fe2+、SO42-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关,下列说法正确的是
A.利用粮食酿酒经历了淀粉→葡萄糖→乙醇的化学变化过程
B.淀粉、油脂和蛋白质都是高分子化合物
C.煤经过气化和液化等物理变化可转化为清洁燃料
D.聚氯乙烯塑料薄膜可用作食品保鲜膜、一次性食品袋等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出N2的电子式_____。下列能实现人工固氮的是____。
A.闪电 B.在加压降温的条件下使空气中的氮气液化
C.根瘤 D.合成氨车间
(2)实验室通常用加热消石灰与氯化铵固体的方法来制取氨气。写出该反应的化学方程式____。实验室制取氨气的方法有多种,下面的装置和选用的试剂中错误的是____。
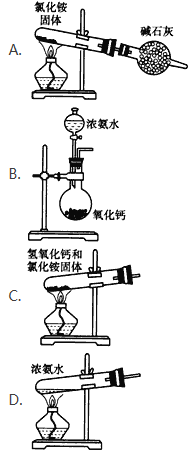
(3)氨气可使湿润的红包石蕊试纸变蓝的原因(用化学用语表示)______。
(4)用乙装置吸收一段时间氨后,再通入空气,同时将加热的铜丝插入乙装置的锥形瓶内,锥形瓶中不可能生成的物质是:____。
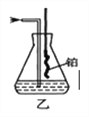
A. H2 B. NO2 C.HNO3 D. NH4N03
写出乙装置中氨催化氧化的化学方程式:______。
(5)已知3Cl2+2NH3→N2+6HCl,常温常压下,在一密闭容器中将15mLCl2和40mLNH3充分反应后,剩余气体的体积为_____mL。
(6)在标准状况下,1L水中可溶解700LNH3,所得溶液的密度为0.9g/cm3,则氨水的物质的量浓度为_____mol/L(保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A. 铁粉溶于稀盐酸:2Fe+6H+=2Fe3++3H2↑
B. 碳酸钙溶于稀盐酸:CO32-+2H+=CO2↑+H2O
C. 氧化铜溶于醋酸:CuO+2CH3COOH =Cu2+ +2CH3COO- +H2O
D. 硫酸铜与氢氧化钡溶液混合:Ba2++SO42-=BaSO4 ↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将6 mol H2和3 mol CO充入容积为0.5 L的密闭容器中,进行如下反应:
2H2(g)+CO(g)![]() CH3OH(g),6秒末时容器内压强为开始时的0.6倍。
CH3OH(g),6秒末时容器内压强为开始时的0.6倍。
试计算:(1)H2的反应速率是多少?(2)CO的转化率为多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com