

| A. | 对羟基扁桃酸可以发生消去反应、取代反应和缩聚反应 | |
| B. | 苯酚和对羟基扁桃酸是同系物 | |
| C. | 乙醛酸与H2在热的镍催化下反应生成乙二醇 | |
| D. | 在核磁共振氢谱中对羟基扁桃酸应该有6个吸收峰 |
分析 A.对羟基扁桃酸中含有酚羟基、苯环、醇羟基和羧基,能发生氧化反应、加成反应、还原反应、取代反应、缩聚反应等;
B.结构相似,在分子组成上相差一个或若干个-CH2原子团的物质互称同系物;
C.乙醛酸与H2在热的镍催化下发生加成反应生成HOCH2COOH;
D.有机物中有几种氢原子其就有几个吸收峰.
解答 解:A.对羟基扁桃酸中连接醇羟基碳原子相邻碳原子上不含氢原子,所以不能发生消去反应,故A错误;
B.苯酚和对羟基扁桃酸结构不相似,所以不是同系物,故B错误;
C.乙醛酸与H2在热的镍催化下发生加成反应生成HOCH2COOH,故C错误;
D.对羟基扁桃酸中氢原子有6类,所以其吸收峰有6个,故D正确;
故选D.
点评 本题考查有机物结构和性质,为高频考查,明确官能团及其性质关系是解本题关键,侧重考查酚、苯、醇和羧酸的性质,易错选项是B,注意同系物定义内涵,题目难度不大.


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | (CH3COO)2Pb+H2S→PbS↓+2CH3COOH | |
| B. | Pb2++2CH3COO-+H2S→PbS↓+2CH3COOH | |
| C. | Pb2++H2S→PbS↓+2H+ | |
| D. | Pb2++2CH3COO-+2H++S2-→PbS↓+2CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHSO3溶液中:c(SO32-)<c(H2SO3) | |
| B. | 吸收过程中,始终存在着:c(Na+)+c(H+)=c(OH-)+2c(SO32-)+c(HSO3-) | |
| C. | 中性溶液中:c(Na+)>c(HSO3-)=c(SO32-)>c(OH-)=c(H+) | |
| D. | 中性溶液中:c(Na+)=c(SO32-)+c(HSO3-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
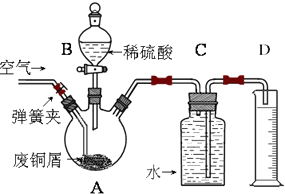 一学习小组利用下图所示装置,对某含少量Fe的废铜屑进行铜含量的测定,并探究利用其制备硫酸铜溶液.
一学习小组利用下图所示装置,对某含少量Fe的废铜屑进行铜含量的测定,并探究利用其制备硫酸铜溶液.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| R | X | |
| T | ||
| Z | Q |
| A. | R的单质结构式为: | |
| B. | 工业上以海水为原料,经氧化还原反应制备Q的单质 | |
| C. | 非金属性:Z<T<X | |
| D. | R原子与Z原子的电子数相差26 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
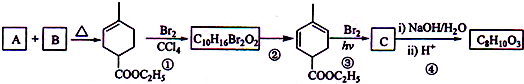
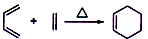
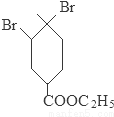 +2NaOH
+2NaOH
 +2NaBr+2H2O;
+2NaBr+2H2O;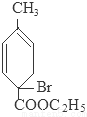 +2H2O
+2H2O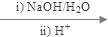
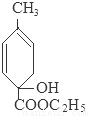 +C2H5OH+HBr:
+C2H5OH+HBr: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中和反应是放热反应 | |
| B. | 右图所示的反应为放热反应 | |
| C. | 化学反应中有物质变化也有能量变化 | |
| D. | 化学键断裂吸收能量,化学键生成放出能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH溶液于水时仅破坏了离子键而未破坏共价键 | |
| B. | NH4Cl溶解于水时不仅破坏了离子键还破坏了共价键 | |
| C. | H2SO4溶解于水时,所有的共价键都被破坏 | |
| D. | HCl溶解于水时电离出H+和Cl-,所以共价键变成了离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O | |
| B. | 若乙池中为足量AgNO3溶液,则阳极的电极反应为:4OH--4e-═2H2O+O2↑ | |
| C. | 若乙池中为一定量CuSO4溶液,通电一段时间后,向所得的溶液中加入0.1molCu(OH)2后恰好恢复到电解前的浓度和pH,则电解过程中转移的电子数为0.2NA | |
| D. | 常温常压下,1gCH3OH燃料生成CO2和液态H2O时放热22.68 kJ,表示该反应的热化学方程式为:CH3OH(l)+1.5O2(g)═CO2(g)+2H2O(l)△H=-725.76 kJ•mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com