
【题目】下列金属中能溶于稀硫酸,但用它制成的容器适合用来盛装浓硫酸的是( )
A.锌 B.铁 C.铜 D.金
科目:高中化学 来源: 题型:
【题目】T℃时,向2 L恒容密闭容器中充入1 mol PCl5,发生反应:PCl5(g) ![]() PCl3(g)+Cl2(g) ,一段时间后达到平衡。部分数据见下表,下列说法正确的是
PCl3(g)+Cl2(g) ,一段时间后达到平衡。部分数据见下表,下列说法正确的是
t / s | 0 | 50 | 150 | 250 | 350 |
n(PCl3) / mol | 0 | 0. 16 | 0. 19 | 0. 2 | 0. 2 |
A.0~50 s内平均速率v(PCl3)= 0. 0032 mol·L-1·s-1
B.其他条件不变,升高温度,平衡时c(PCl3)= 0. 11 mol·L-1,则反应的△H<0
C.相同温度下,起始时向容器中充入1mol PCl5、0. 2 mol PCl3 和0. 2 mol Cl2,反应达到平衡前v(正)>v(逆)
D.相同温度下,起始时向容器中充入2 mol PCl3 、2 mol Cl2,达到平衡时PCl3 的转化率小于80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有甲、乙两个完全相同的装置,分别在它们的侧管中装入1.06 g Na2CO3和0.84 g NaHCO3,试管中各有10 mL相同浓度的盐酸(如下图),同时将两个侧管中的物质 全部倒入各自的试管中,下列叙述正确的是

A.甲装置的气球膨胀速率大
B.若最终两气球体积相同,则一定有c(HCl)≥2molL-1
C.若最终两气球体积不同,则一定有c(HCI)≤lmolL-1
D.最终两溶液中Na+、C1-的物质的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中,充入1mol N2 和3 mol H2,并在一定温度和压强条件下,使其发生反应:N2(g) + 3H2 (g) ![]() 2NH3(g) △H=-92.4 kJ/mol
2NH3(g) △H=-92.4 kJ/mol
(1)若保持容器体积不变,再向其中充入1mol N2,反应速率会_________(填“加快”、“减慢”或“不变”),理由是______________________。
(2)若保持容器体积不变,再向其中充入1mol氩气,反应速率会_________(填“加快”、“减慢”或“不变”),理由是_______________________。
(3)若保持容器气体压强不变,再向其中充入1mol N2 和3 mol H2,反应速率会_________(填“加快”、“减慢”或“不变”),理由是____________________。
(4)使用催化剂,反应速率会_________(填“加快”、“减慢”或“不变”),理由是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。下列分析正确的是( )
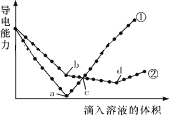
A.②代表滴加H2SO4溶液的变化曲线
B.b点溶液中大量存在的离子是SO42-、Na+、OH-
C.a、d两点对应的溶液均显中性
D.c点两溶液中含有相同量的OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)完全燃烧一定质量的无水乙醇,放出的热量为QkJ,为完全吸收生成的CO2,并使之生成正盐,消耗0.8mol/L NaOH溶液50mL,则燃烧1mol酒精放出的热量是_________________。
(2)白磷与氧可发生如下反应:P4+5O2=P4O10。
已知断裂下列化学键需要吸收的能量分别为:
P-P akJ·mol-1、P-O bkJ·mol-1、
P=O ckJ·mol-1、O=O dkJ·mol-1
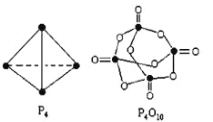
根据图示的分子结构和有关数据计算该反应的反应热__________________。
(3)现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H=-24.8kJ/mol
3Fe2O3(s)+ CO(g)=2Fe3O4(s)+ CO2(g) △H=-47.2kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=-19.4kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝是一种新型的无机非金属材料,被广泛应用于集成电路生产领域.其制备反应原理为:Al2O3+N2+3C═2AlN+3CO.制备过程中,原料配比不当或反应不完全等因素都会造成产品中含有碳或Al2O3等杂质.为测定产品中AlN的质量分数,某同学按如图1装置进行相关实验.可选用的化学试剂为:mg氮化铝片状固体、NaOH饱和溶液、水、煤油、医用酒精.回答下列问题:

(1)组装完实验装置,使用前第一步应该
(2)图1(B)中试剂最好选用 (填序号):
①煤油 ②医用酒精 ③水
已知A 中有NaAlO2生成,并放出有刺激性气味气体,写出A中发生反应的离子方程式 .
(3)读取C(量筒)中液体体积时,应注意下列问题,错误的是 (填序号)
a.C中液面不再上升时立即读数
b.上下移动C,使之液面与B中液面相平
c.A中不再有气泡逸出
d.视线与凹液面最低处相平
(4)mg氮化铝与足量NaOH饱和溶液反应,实验结束后,C中收集到液体的体积为VL(已折算成标准状况),则AlN样品的纯度为 (写计算表达式).
(5)上述实验方案,可能因气体体积测量不准,导致误差较大.有人建议改用下列A、B两个装置中的一种(在通风橱内进行),只需进行简单而又必要的数据测写,用差量法就可比较准确确定样品中AlN的质量分数.较合理的装置是: (填代号).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知方程式2H2(g)+O2(g)=2H2O(l)ΔH1=-571.6kJ·mol-1,则关于方程式2H2O(l)=2H2(g)+O2(g)ΔH2=?的说法中正确的是( )
A.方程式中化学计量数表示分子数
B.该反应的ΔH2=-571.6kJ·mol-1
C.该反应ΔH2大于零
D.该反应可表示18g水分解时的热效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.水库中的钢闸门通常连接锌块,是采用了牺牲阳极的阴极保护法
B.化学电源都是一次能源
C.铁的表面镀铜的过程中,铜极连接电源负极
D.合金的熔点都高于它的成分金属,合金的耐腐蚀性也都比其组成成分金属强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com