
Ⅰ.铁盐、亚铁盐是实验室常用的药品。
请根据题意,完成下列填空:
(1)向酸化的FeCl3溶液中逐滴加入KI溶液,溶液变成棕褐色。该反应的离子方程式为________________。
(2)向酸化的FeSO4溶液中加几滴硫氰化钾溶液,没有什么明显变化,再滴加双氧水,溶液变血红色。继续滴加双氧水,血红色逐渐褪去,且有气泡产生。
写出上述变化中,有关反应的离子方程式:
①____________________________________;
②Fe3++3SCN-=Fe(SCN)3;
③11H2O2+2SCN-=2SO42—+2CO2↑+N2↑+10H2O+2H+
若生成1 mol N2,H2O2和SCN-的反应中转移电子的物质的量是________ mol。
(3)根据以上实验,推断Fe2+、I-和SCN-的还原性由强到弱的顺序为________。
Ⅱ.某课题组利用Fe粉和KNO3溶液反应,模拟地下水脱氮过程,探究脱氮原理。
(4)实验前:①先用0.1 mol·L-1 H2SO4洗涤Fe粉,其目的是__________,然后用蒸馏水洗涤至中性;②将KNO3溶液的pH调至2.5;③为防止空气中的O2对脱氮的影响,应向KNO3溶液通入________(写化学式)。
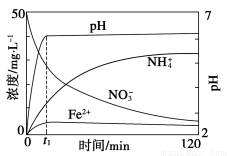
(5)如图表示足量Fe粉还原上述KNO3溶液过程中,测出的溶液中相关离子浓度、pH随时间的变化关系(部分副反应产物曲线略去)。请根据图中信息写出t1时刻前该反应生成的阳离子分别是________、________。t1时刻后,该反应仍在进行,溶液中NH4+的浓度在增大,Fe2+的浓度却没有增大,可能的原因是__________________。
Ⅰ.(1)2Fe3++2I-=2Fe2++I2
(2)2Fe2++H2O2+2H+=2Fe3++2H2O 22
(3)I->Fe2+>SCN-
Ⅱ.(4)除去Fe粉表面的铁锈(Fe2O3)等杂质 N2
(5)Fe2+、NH4+ 溶液的pH增大,Fe2+形成了Fe(OH)2(或与溶液中OH-结合)
【解析】(1)Fe3+能氧化I-,离子方程式为2Fe3++2I-=2Fe2++I2。
(2)Fe2+和SCN-不反应,当加入H2O2时,发生2Fe2++2H++H2O2=2Fe3++2H2O,然后Fe3+和SCN-反应生成血红色溶液,继续滴加H2O2,SCN-被氧化。根据反应③,当有1 mol N2生成时,转移电子的物质的量为11×2×[-1-(-2)] mol=22 mol。(注:根据氧化剂计算方便)
(3)根据(1)(2)中方程式可得还原性I->Fe2+>SCN-。(根据还原剂还原性大于还原产物还原性)
(4)因为Fe粉表面有铁锈,所以应预先用H2SO4除去。因为Fe粉在溶液中能被O2氧化,所以应通入N2排除O2的干扰。
(5)根据图中信息,Fe粉被NO3—氧化成Fe2+,其本身被还原成NH4+,在此过程中碱性增强,因为有OH-生成,Fe2+与之反应生成Fe(OH)2沉淀,造成Fe2+的浓度变化不大。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014高考化学二轮复习限时集训 专题10非金属元素单质及化合物练习卷(解析版) 题型:选择题
已知X、Y在一定条件下发生反应,可以得到E、F、G。下列假设与结论能对应成立的是( )
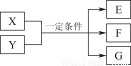
选项假设结论
A若X、Y均为固体,E为气体则E一定能使湿润的蓝色石蕊试纸变红
B 若该反应是氯碱工业的主要反应,反应一段时间后两极产生的气体体积可能不同(不考虑气体的溶解)
C若X为单质,Y为氧化性酸,气体E是能引起酸雨的主要物质则Y一定是浓H2SO4
D若X为有机物,得到E是一种红色沉淀则X一定是醛
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮专题突破 专题十四常见有机物及其应用练习卷(解析版) 题型:选择题
间二甲苯的一氯代物的同分异构体有( )
A.4种 B.3种 C.2种 D.1种
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮专题突破 专题十二常见非金属元素练习卷(解析版) 题型:填空题
在下列物质转化关系中,反应的条件和部分产物已略去。
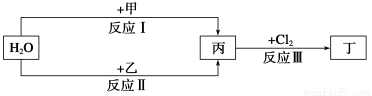
回答下列问题:
(1)若甲、乙是两种常见金属,反应Ⅲ是工业制盐酸的反应。
①反应Ⅰ中,甲在通常条件下和水剧烈反应,除丙外,还生成一种焰色反应为黄色的物质,则工业上生产甲的一般方法是________(填字母)。
A.热分解法 B.热还原法 C.电解法
②反应Ⅱ中,乙与H2O在高温下反应,除丙外,还生成一种有磁性的物质,则反应Ⅱ的化学方程式是______________________________________。
③通过比较反应Ⅰ、Ⅱ的反应条件,可得出甲的金属性比乙的金属性________(填“强”或“弱”),比较二者金属性强弱的依据还可以是(写出一种即可)__________________。
(2)若甲、乙是化合物,且反应Ⅲ是工业制漂白粉的反应。
①反应Ⅲ的化学方程式是__________________________________________________。
②反应Ⅰ的另一种产物为有机物,则该有机物的电子式是______________。
③在饱和氯水中加块状石灰石,能制得较浓HClO溶液,同时放出一种气体。其反应的离子方程式是______________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮专题突破 专题十二常见非金属元素练习卷(解析版) 题型:选择题
某化学小组用下图所示装置制取氯气,下列说法不正确的是( )
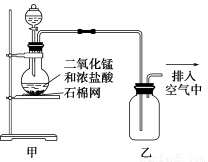
A.该装置图中至少存在两处明显错误
B.烧瓶中的MnO2可换成KMnO4
C.在乙后连一盛有饱和食盐水的烧杯可进行尾气处理
D.在集气瓶的导管口处放一片湿润的淀粉?KI试纸可以证明是否有氯气逸出
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮专题突破 专题十七有机化学基础练习卷(解析版) 题型:填空题
乙基香草醛(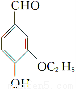 )是食品添加剂的增香原料。
)是食品添加剂的增香原料。
(1)写出乙基香草醛分子中任意两种含氧官能团的名称______________________。
(2)与乙基香草醛互为同分异构体,能与NaHCO3溶液反应放出气体,且苯环上只有一个侧链(不含R—O—R′及R—O—COOH结构)的有________种。
(3)A是上述同分异构体中的一种,可发生以下变化:
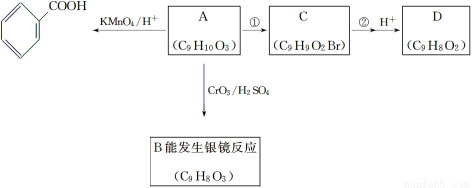
已知:ⅰ.RCH2OH 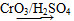 RCHO;
RCHO;
ⅱ.与苯环直接相连的碳原子上有氢时,此碳原子才可被酸性KMnO4溶液氧化为羧基。
a.写出A的结构简式:___________________________,
反应②发生的条件是______________________________。
b.由A可直接生成D,反应①和②的目的是_________________________。
c.写出反应方程式:A→B______________________________。
C与NaOH水溶液共热:___________________________________。
(4)乙基香草醛的另一种同分异构体E
( )是一种医药中间体。由茴香醛(
)是一种医药中间体。由茴香醛( )合成E(其他原料自选),涉及的反应类型有(按反应顺序填写)________________________。
)合成E(其他原料自选),涉及的反应类型有(按反应顺序填写)________________________。
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮专题突破 专题十一常见金属元素练习卷(解析版) 题型:实验题
某化学小组在学习元素周期律后,对教材中Fe2+氧化为Fe3+的实验进一步思考,并提出问题:Cl2能将Fe2+氧化为Fe3+,那么Br2和I2能否将Fe2+氧化为Fe3+?
环节一:理论推测
部分同学认为Br2和I2都可能将Fe2+氧化为Fe3+,他们思考的依据是________。
部分同学认为Br2和I2都不能将Fe2+氧化为Fe3+,还有同学认为Br2能将Fe2+氧化为
Fe3+而I2不能。他们思考的依据是从上到下卤素单质氧化性减弱。
环节二:设计实验进行验证
在大试管中加适量铁粉,加入10 mL稀盐酸,振荡试管,充分反应后,铁粉有剩余,取上层清液进行下列实验:。
实验1:
试管 | 操作 | 现象 |
① | 先向试管中加入2 mL FeCl2溶液,再滴加少量红棕色的溴水,振荡试管 | 溶液为黄色 |
② | 先向试管中加入2 mL FeCl2溶液,再滴加少量棕黄色的碘水,振荡试管 | 溶液为黄色 |
环节三:实验现象的分析与解释
(1)同学甲认为①中现象说明溴水能将Fe2+氧化,离子方程式为________。
同学乙认为应该补充实验,才能得出同学甲的结论。请你帮助同学乙完成实验:
实验2:
操作 | 应该观察到的现象 |
(2)该小组同学对②中溶液呈黄色的原因展开了讨论:
可能1:碘水与FeCl2溶液不反应,黄色是碘水稀释后的颜色。
可能2:______________。
实验3:进行实验以确定可能的原因。
操作 | 现象 |
向试管②所得溶液中继续加入0.5 mL CCl4,充分振荡,静置一段时间后。取出上层溶液,滴KSCN溶液 | 静置后,上层溶液几乎无色,下层溶液为紫色;上层溶液滴加KSCN溶液后,出现浅红色 |
同学丙认为该实验现象可以说明是“可能2”成立,同学丁认为不严谨,于是设计了实验4:
实验4:
操作 | 现象 |
向另一支试管中加入2 mL FeCl2溶液,滴加0.5 mL碘水后,再加入0.5 mL乙酸乙酯,充分振荡,静置一段时间后。取出下层溶液,滴加KSCN溶液 | 静置后,上层溶液为紫色,下层溶液几乎无色;下层溶液滴加KSCN溶液后,没有出现浅红色 |
你认为实验4设计的主要目的是________________。
同学丁根据实验4现象得出结论:在本次实验条件下,碘水与FeCl2溶液反应的程度很小。
(3)Cl2、Br2、I2氧化Fe2+的能力逐渐减弱,用原子结构解释原因:__________。
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮专题突破 专题六物质结构和元素周期律练习卷(解析版) 题型:填空题
现有七种短周期主族元素,其原子序数按A、B、C、D、E、F、G的顺序递增。A元素的最高正化合价和最低负化合价的代数和等于0,且A是形成化合物种类最多的元素;C原子能形成分别含10电子、18电子的两种阴离子,且C与F位于同一主族;D单质投入冷水中反应缓慢,投入沸水中迅速产生气泡;E的简单阳离子是同周期元素所形成的简单离子中半径最小的。回答下列问题:
(1)B位于周期表第________周期第________族。
(2)A、B、C三种元素能形成等电子体,请写出其中一组等电子体:________________________________________________________________________。
(3)元素M位于E与F元素之间,且M单质是优良的半导体材料,广泛用于太阳能电池。M、F、G的气态氢化物的稳定性由强到弱的顺序为______________(用化学式表示)。
(4)若选择三种试剂设计实验能证明非金属性:B>A>M,用化学方程式表示实验原理:__________________________________________________。
(5)A、M、F、G的最高价氧化物对应水化物的酸性由强到弱的顺序为________________________(用化学式表示)。
(6)下列实验方法能证明D与E的金属性强弱关系的是________(填字母序号)。
A.比较D和E的单质分别与稀硫酸反应产生气泡的快慢
B.比较D和E的单质分别与同浓度的氢氧化钠溶液反应产生气泡的快慢
C.比较D和E的单质分别与氯气、氧气、硫等非金属单质反应的产物
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮专题突破 专题二化学用语及常用计量练习卷(解析版) 题型:选择题
在下列条件下,两种气体的分子数一定相等的是( )
A.同温度、同体积的N2和O2
B.同质量、不同密度的N2和CO
C.同压强、同体积的H2和CH4
D.同体积、同密度的CO2和N2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com