
| A. | 相同物质的量浓度的溶液:①(NH4)2SO4 ②NH4HCO3 ③NH4Cl ④NH3•H2O中,c(NH4)由大到小的顺序是:①>③>②>④ | |
| B. | 将等体积的盐酸和氨水混合后pH=7:c(NH4+)>c(Cl-) | |
| C. | 0.1 mol•L-1Na2CO3溶液中:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3) | |
| D. | 向硝酸钠溶液中滴加稀盐酸得到pH=5的混合溶液:c(Na+)=c(NO3-)+c(Cl-) |
分析 A.物质的量相等的这几种溶液中,NH3•H2O溶液中c(NH4+)小于铵盐的c(NH4+),铵根离子水解程度较小,所以要比较铵根离子浓度大小,先比较盐中铵根离子的系数,系数越大,溶液中铵根离子浓度越大,相同系数的铵盐溶液,再根据溶液中其它离子是促进铵根离子水解还是抑制铵根离子水解判断即可;
B.混合溶液呈中性,则c(H+)=c(OH-),再结合电荷守恒判断;
C.0.1 mol•L-1Na2CO3溶液中存在质子守恒,水电离出氢离子浓度和氢氧根离子浓度相同;
D.pH=5的混合溶液,钠离子、硝酸根离子不电离、不水解.
解答 解:NH3•H2O溶液中c(NH4+)小于铵盐的c(NH4+),所以一水合氨溶液中铵根离子浓度最小;②③中铵根离子系数都是1,碳酸氢根离子促进铵根离子水解,c(NH4)③>②;①中铵根离子系数都是2,其溶液中铵根离子浓度大于其余溶液中铵根离子浓度,则溶液中铵根离子浓度从小到大顺序是:①>③>②>④,故A正确;
B.常温下若一定量的氨水和盐酸混合后溶液的PH=7,溶液呈中性,则c(H+)=c(OH-),根据电荷守恒得c(NH4+)=c(Cl-),故B错误;
C.0.1 mol•L-1Na2CO3溶液中存在质子守恒:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3),故C错误;
D.向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液中c(Na+)=c(NO3-),故D错误;
故选A.
点评 本题考查离子浓度大小的比较,明确盐类水解的应用及质子守恒、电荷守恒即可解答,注意选项D为易错点,题目难度中等.


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2-乙基-1,3-丁二烯的键线式: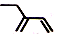 | |
| B. | 等物质的量的苯和苯甲酸完全燃烧消耗氧气的量相等 | |
| C. | 苯与甲苯互为同系物,均能使KMnO4酸性溶液褪色 | |
| D. | 用溴水可鉴别苯、CCl4、苯乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
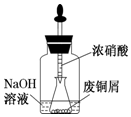 由废铜制硝酸铜.用胶头滴管吸取浓HNO3缓慢加到锥形瓶内的废铜屑中(废铜屑过量),充分反应后过滤,得到硝酸铜溶液.
由废铜制硝酸铜.用胶头滴管吸取浓HNO3缓慢加到锥形瓶内的废铜屑中(废铜屑过量),充分反应后过滤,得到硝酸铜溶液.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐酸、氢氧化钠醋酸、干冰 | B. | 澄清的石灰水、铜、氨气 | ||
| C. | 石油、水、硫酸钡 | D. | 海水、氯化钠、氧气 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ag+、Cu2+、Cl-、NO3- | B. | Fe2+、NH4+、CO32-、OH- | ||
| C. | Na+、Cl-、K+、OH- | D. | H+、K+、Fe3+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某温度下,将等物质的量的A、B、C、D四种物质混合于一恒容密闭容器中,发生如下反应:aA(g)+bB(g)?cC(g)+dD(s),(正反应为放热反应).当反应进行一段时间后,测得A减少了n mol,B减少了n/2mol,C增加了3n/2mol,D增加了n mol,此时达到化学平衡状态.则下列说法正确的是( )
某温度下,将等物质的量的A、B、C、D四种物质混合于一恒容密闭容器中,发生如下反应:aA(g)+bB(g)?cC(g)+dD(s),(正反应为放热反应).当反应进行一段时间后,测得A减少了n mol,B减少了n/2mol,C增加了3n/2mol,D增加了n mol,此时达到化学平衡状态.则下列说法正确的是( )| A. | 达到化学平衡时A的消耗速率与C的消耗速率相等 | |
| B. | 保持温度不变,再向容器中充入n mol A和$\frac{n}{2}$molB,平衡不移动 | |
| C. | 保持温度不变,再向容器中充入n mol A和n mol B,A、B的转化率均不变 | |
| D. | 如图表示该反应的正反应速率随时间的变化情况,t1时刻可能是减小了A的浓度,增加了C的浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1000 mL,212 g | B. | 950 mL,201.4 g | C. | 500 mL,286 g | D. | 1000 mL,201.4 g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com