
【题目】下列叙述正确的是
A. 用冰冷却苯,苯可以凝结成无色的晶体
B. 苯与溴水混合后因发生反应而使溴水褪色
C. 在苯中加入酸性 KMnO4溶液,振荡后静置,上层液体为紫红色
D. 1 mol 苯能与 3 mol H2发生加成反应,说明在苯环中含有 3 个双键
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案科目:高中化学 来源: 题型:
【题目】CH4、H2、C都是优质的能源物质,它们燃烧的热化学方程式为:
①CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1
②2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
③C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
(1)在深海中存在一种甲烷细菌,它们依靠酶使甲烷与O2作用产生的能量存活,甲烷细菌使1 mol甲烷生成CO2气体与液态水,放出的能量____________(填“>”“<”或“=”)890.3 kJ。
(2)甲烷与CO2可用于合成合成气(主要成分是一氧化碳和氢气):CH4+CO2=2CO+2H2,1 g CH4完全反应可释放15.46 kJ的热量,则:
①能表示该反应过程中能量变化的是____________(填字母)。

②若将物质的量均为1 mol的CH4与CO2充入某恒容密闭容器中,体系放出的热量随着时间的变化如图所示,则CH4的转化率为____________。

(3)C(s)与H2(g)不反应,所以C(s)+2H2(g)=CH4(g)的反应热无法直接测量,但通过上述反应可求出C(s)+2H2(g)=CH4(g)的反应热ΔH=____________。
(4)目前对于上述三种物质的研究是燃料研究的重点,下列关于上述三种物质的研究方向中可行的是_______________(填字母)。
A.寻找优质催化剂,使CO2与H2O反应生成CH4与O2,并放出热量
B.寻找优质催化剂,在常温常压下使CO2分解生成碳与O2
C.寻找优质催化剂,利用太阳能使大气中的CO2与海底开采的CH4合成合成气(CO、H2)
D.将固态碳合成为C60,以C60作为燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.含碳元素的化合物都是有机物
B.完全燃烧只生成 CO2和 H2O 的化合物都是烃
C.有机物完全燃烧只可能生成 CO2 和 H2O
D.点燃混有空气的甲烷不一定会爆炸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.某温度时,在一个容积为2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
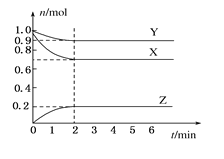
(1)该反应的化学方程式为_______________________。
(2)反应开始至2 min,气体Z的平均反应速率为____________。
(3)若X、Y、Z均为气体,反应达到平衡时:
①压强是开始时的____________倍;
②若此时将容器的体积缩小为原来的![]() 倍,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为____________反应(填“放热”或“吸热”)。
倍,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为____________反应(填“放热”或“吸热”)。
Ⅱ.某科研小组欲研究在其他条件不变的情况下,改变起始氧气的物质的量对合成新型硝化剂反应:4NO2(g)+O2(g)![]() 2N2O5(g) ΔH<0的影响。
2N2O5(g) ΔH<0的影响。

(1)图像中T1和T2的关系是T1________T2(填“>”、“<”或“=”);
(2)比较a、b、c三点所处的平衡状态中,反应物NO2的转化率最大的是__________(填字母);
(3)若容器体积为1 L,n=1 mol,NO2的转化率为50%,则此条件下(T2),反应的平衡常数K=___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去下列物质中所含少量杂质的方法正确的是
选项 | 物质 | 杂质 | 试剂 | 提纯方法 |
A | 乙醛 | 乙酸 | NaOH溶液 | 蒸馏 |
B | 苯 | 苯酚 | 浓溴水 | 过滤 |
C | 乙酸乙酯 | 乙酸 | NaOH溶液 | 混合振荡、静置分液 |
D | 乙烷 | 乙烯 | 氢气 | 催化剂、加热 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在NaCl、MgCl2、MgSO4形成的混合溶液中,c(Na+)=0.1mol/L,c(Mg2+)=0.25mol/L,c(Cl﹣)=0.2mol/L,则c(SO42﹣)为( )
A.0.15 mol/L
B.0.10 mol/L
C.0.25 mol/L
D.0.20 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是CO2电催化还原为CH4的工作原理示意图。下列说法不正确的是
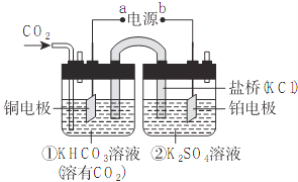
A.该过程是电能转化为化学能的过程
B.铜电极的电极反应式为CO2+8H++8e-=CH4+2H2O
C.一段时间后,①池中n(KHCO3)不变
D.一段时间后,②池中溶液的pH不一定升高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com