
(1)等质量的O2、CH4、H2的物质的量的比值为 .
38g某二价金属氯化物(ACl2)中含有0.8mol Cl﹣,则ACl2的摩尔质量是 ;A的相对原子质量是 ;ACl2的化学式是 .
(3)新制备的氯水显 色,说明氯水中有 (填分子式)分子存在.
(4)向氯水中滴加几滴AgNO3溶液,立即有 生成,说明氯水中有 (填离子符号)存在,反应的化学方程式为 氯水光照后颜色变浅,并放出 气体.
考点: 物质的量的相关计算.
专题: 计算题.
分析: (1)根据n=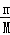 计算;
计算;
根据该金属氯化物的化学式及氯离子的物质的量可以计算出该金属氯化物的物质的量,然后根据M=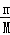 计算出ACl2的摩尔质量,从而可知A的相等原子质量,确定A为镁元素;
计算出ACl2的摩尔质量,从而可知A的相等原子质量,确定A为镁元素;
(3)氯气为黄绿色气体,微溶于水;
(4)氯水中,氯气与水反应:Cl2+H2O⇌HCl+HClO,结合溶液中粒子的成分及性质解答;HClO不稳定,见光易分解;
解答: 解:(1)设质量都为1g,则等质量的O2、CH4、H2的物质的量的比值为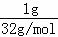 :
: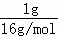 :
: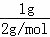 =1:2:16,
=1:2:16,
故答案为:1:2:16;
38g某二价金属的氯化物ACl2中含有0.8mol Cl﹣,则ACl2的物质的量为:n(ACl2)=0.8mol×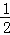 =0.4mol,ACl2的摩尔质量为:M(ACl2)=
=0.4mol,ACl2的摩尔质量为:M(ACl2)= =95g/mol;即ACl2的相对分子量为:95,所以A的相对原子量为95﹣35.5×2=24,A为镁元素,所以ACl2的化学式是MgCl2,
=95g/mol;即ACl2的相对分子量为:95,所以A的相对原子量为95﹣35.5×2=24,A为镁元素,所以ACl2的化学式是MgCl2,
故答案为:95g/mol;24;MgCl2;
(3)氯气为黄绿色气体,微溶于水,新制备的氯水显黄绿色,是由于氯水中有Cl2,
故答案为:黄绿;Cl2;
(4)氯水显黄绿色,是由于氯水中有Cl2,氯气与水发生Cl2+H2O⇌H++Cl﹣+HClO,溶液中含有Cl﹣,加入几滴AgNO3溶液,发生Cl﹣+Ag+=AgCl↓,生成白色沉淀,HClO不稳定,见光易分解,反应为:2HClO 2HCl+O2↑,光照条件下溶液颜色逐渐变浅,并有无色气泡O2产生,
2HCl+O2↑,光照条件下溶液颜色逐渐变浅,并有无色气泡O2产生,
故答案为:白色沉淀;Cl﹣;Cl2+H2O=H++Cl﹣+HClO、Cl﹣+Ag+=AgCl↓;O2;
点评: 本题考查物质的量的计算、氯气的性质,为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意相关计算公式的运用,注意氯气的颜色、水溶性以及HClO的性质.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列各组中的性质比较中,不正确的是( )
|
| A. | 酸性 HClO4>HBrO4>HIO4 | B. | 碱性Ba(OH)2>Ca(OH)2>Mg(OH)2 |
|
| C. | 还原性 F﹣>Cl﹣>Br﹣ | D. | 稳定性 HCl>H2S>PH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
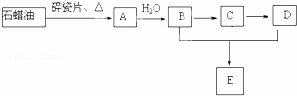
A是一种重要的化工原料,A的产量可以用来衡量一个国家的石油化工水平,E(C4H8O2)是具有果香气味的液体.A、B、C、D在一定条件下有如下转化关系(部分反应条件、产物被省略)
(1)A→B的反应类型是 ;B、D中官能团的名称分别是 、 ;
(2)写出反应B→C的化学方程式: .
(3)丁烷是由石蜡油获得A的过程中的中间产物之一,它的一种同分异构体中含有三个甲基,则这种同分异构体的结构简式: .
(4)人在做过剧烈运动后,有一段时间腿和胳膊感到有酸胀或疼痛的感觉.原因之一是:C6H12O6 2C3H6O3.已知乳酸分子中含有与B、D中相同的官能团,且有一个甲基,则乳酸的结构简式是 ,90g乳酸与足量金属钠完全反应产生的气体在标准状况下的体积是 L.
2C3H6O3.已知乳酸分子中含有与B、D中相同的官能团,且有一个甲基,则乳酸的结构简式是 ,90g乳酸与足量金属钠完全反应产生的气体在标准状况下的体积是 L.
查看答案和解析>>
科目:高中化学 来源: 题型:
保护环境是每一个公民的责任,下列做法有利于保护环境的是( )
①推广使用无磷洗涤剂 ②城市生活垃圾分类处理 ③推广使用一次性木质筷子 ④推广使用清洁能源 ⑤过量使用化肥、农药 ⑥推广使用无氟冰箱.
A. ①②④⑤ B. ②③④⑥ C. ①②④⑥ D. ③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A. 64g SO2中含有的氧原子数为2NA
B. 含有6.02×1023个H原子的H2在标准状况下的体积约为22.4L
C. 40g NaOH溶解在1L水中,所制得的溶液,物质的量浓度为1mol•L﹣1
D. 标准状况下,11.2L H2O含有的分子数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
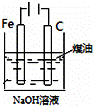
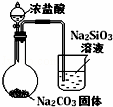
下列图中的实验方案,能达到实验目的是()
A B C D
实验
方案 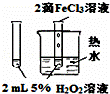

实验
目的 验证FeCl3对H2O2分解反应有催化作用 制备Fe(OH)2并能较长时间观察其颜色 除去CO2气体中混有的SO2 比较HCl、H2CO3和H2SiO3的酸性强弱
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学在实验室从如图I标签的试剂瓶中取少许钠进行燃烧实验,实验后发现还有少许黑色固体生成.从反应物及实验操作猜测:该黑色物质可能为炭与另一种氧化物组成的混合物.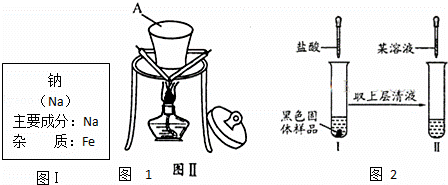
根据题意和图示回答下面问题:
(1)装置图Ⅱ中A的名称
(2)此氧化物可能是FeO或 (写化学式)
(3)对黑色固体物质的组成作如图所示探究
①实验I加入盐酸溶液的目的是 ;
②仅通过实验Ⅱ,用最简步骤能快速确定
黑色氧化物的组成,请完善该设计.(限选试剂:稀盐酸、KSCN溶液、10%H2O2 溶液)
实验操作 预期现象与结论 相关离子方程式
取少量实验Ⅰ中的澄清溶液,加入试剂 . .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应mX(g)+nY(g)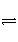
 qZ(g)的ΔH<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是( )
qZ(g)的ΔH<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是( )
A.通入稀有气体使压强增大,平衡将正向移动
B.X的正反应速率是Y的逆反应速率的m/n倍
C.降低温度,混合气体的平均相对分子质量变小
D.增加X的物质的量,Y的转化率降低
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH1=-Q1 kJ·mol-1
2H2(g)+O2(g)===2H2O(g) ΔH2=-Q2 kJ·mol-1
2H2(g)+O2(g)===2H2O(l) ΔH3=-Q3 kJ·mol-1
常温下,取体积比4∶1的甲烷和氢气的混合气体11.2 L(标准状况下),经完全燃烧后恢复至室温,则放出的热量为( )
A.0.4Q1+0.05Q3 B.0.4Q1+0.05Q2
C.0.4Q1+0.1Q3 D.0.4Q1+0.2Q2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com