
【题目】A、B、C、D、E是原子序数依次增大的短周期元素,A是短周期中金属性最强的元素,B是地壳中含量最高的金属元素,C单质的晶体是良好的半导体材料,D的最外层电子数与内层电子数之比为3:5。
(1)C的原子结构示意图为______,D在元素周期表中的位置______。
(2)A单质在氧气中燃烧生成化合物甲,甲中所含化学键为________;A单质在E单质中燃烧生成化合物乙,用电子式表示乙的形成过程__________________。
(3)F是中学化学常见元素,它的一种氧化物为红棕色粉末,B单质与其在高温条件下反应是冶炼F单质的方法之一,该反应的化学方程式为________________。
(4)E元素的非金属性强于D元素,用原子结构解释原因:同周期元素随着原子序数的递增,______________________________,非金属性增强。
(5)工业上将干燥的E单质通入D熔融的单质中可制得化合物D2E2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为__________________。
【答案】 第3周期,第VIA族离子键、非极性共价键
第3周期,第VIA族离子键、非极性共价键![]() Fe2O3+2Al
Fe2O3+2Al![]() 2Fe+Al2O3原子半径递减,得电子能力增强2S2Cl2﹢2H2O=3S+SO2↑+4HCl
2Fe+Al2O3原子半径递减,得电子能力增强2S2Cl2﹢2H2O=3S+SO2↑+4HCl
【解析】
A、B、C、D、E是原子序数依次增大的短周期元素,A是短周期中金属性最强的元素,则A是钠元素,B是地壳中含量最高的金属元素,则B是铝元素,C单质的晶体是良好的半导体材料,则C为硅元素,D的最外层电子数与内层电子数之比为3:5,则D为硫元素,所以E为氯元素,据此解答。
根据以上分析可知A是Na,B是Al,C是Si,D是S,E是Cl。则
(1)C为硅元素,C的原子结构示意图为![]() ,D为硫元素,D在元素周期表中的位置是第三周期第VIA族。
,D为硫元素,D在元素周期表中的位置是第三周期第VIA族。
(2)钠单质在氧气中燃烧生成化合物甲为过氧化钠,甲中所含化学键为离子键、非极性共价键;钠单质在氯气中燃烧生成化合物乙为氯化钠,氯化钠属于离子化合物,其形成过程为![]() 。
。
(3)F是中学化学常见元素,它的一种氧化物为红棕色粉末,B单质与其在高温条件下反应是冶炼F单质的方法之一,该反应为铝热反应,则F为铁元素,因此该反应的化学方程式为Fe2O3+2Al![]() 2Fe+Al2O3。
2Fe+Al2O3。
(4)氯元素的非金属性强于硫元素,这是由于同周期元素随着原子序数的递增,原子半径递减,得电子能力增强,非金属性增强。
(5)工业上将干燥的E单质通入D熔融的单质中可制得化合物为S2Cl2,该物质可与水反应生成一种能使品红溶液褪色的气体为SO2,0.2mol该物质参加反应时转移0.3mol电子,则1molS2Cl2参加反应要转移1.5mol电子,其中只有一种元素化合价发生改变,则应为硫元素的化合价在改变,因此该反应的化学方程式为2S2Cl2+2H2O=3S+SO2↑+4HCl。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】合成氨是人类科学技术上的一项重大突破,是化学和技术对社会发展与进步的巨大贡献之一。在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒。除去CO的化学反应方程式(HAc表示醋酸): Cu(NH3)2Ac+CO+NH3==Cu(NH3)3 (CO) Ac。
请回答下列问题:
(1)C、N、O的第一电离能由大到小的顺序为________。
(2)配合物Cu(NH3)3 (CO) Ac中心原子的配位数为________,基态铜原子核外电子排布式为_________________。
(3)写出与CO互为等电子体的粒子________ (任写一个) 。
(4)在一定条件下NH3与CO2能合成化肥尿素[CO(NH2)2],尿素中,C原子轨道的杂化类型为________;1 mol尿素分子中,σ键的个数为____________。(设NA为阿伏加德罗常数的值)
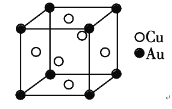
(5)铜金合金形成的晶胞如图所示,其中Cu、Au原子个数比为________。铜单质晶胞与铜金合金的晶胞相似,晶胞边长为3.61×10-8cm,则铜的密度为________g/cm-3(结果保留3位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是甲、乙、丙三位同学制备乙酸乙酯的过程,请你参与并协助他们完成相关实验任务。
(实验目的) 制取乙酸乙酯
(1).(实验原理) 甲、乙、丙三位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯,浓硫酸作吸水剂和__________。
(2).(装置设计)甲、乙、丙三位同学分别设计了下列三套实验装置:

请从甲、乙两位同学设计的装置中选择一种作为实验室制取乙酸乙酯的装置,应选择的装置是______(填“甲”或“乙”)。丙同学将甲装置中的玻璃管改成了球形干燥管,除起冷凝作用外,另一重要作用是__________。
(实验步骤)
①按你选择的装置组装仪器,在试管中先加入3mL乙醇,然后边振荡试管①边慢慢加入2mL浓H2SO4和2mL乙酸;
②将试管①固定在铁架上;
③在试管②中加入适量的饱和Na2CO3溶液;
④用酒精灯对试管①缓慢加热;
⑤当观察到试管②中有明显现象时停止实验。
(3).(问题讨论)
a.步骤(1)装好实验装置,加入样品前还应检查__________;
b.根据试管②中观察到的现象,可知乙酸乙酯的物理性质有:无色油状液体、__________;
c.试管②中分离出乙酸乙酯的实验操作是__________。
d.写出制备乙酸乙酯的化学方程式:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,平衡pH值随溶液体积变化的曲线如图所示。

据图判断正确的是
A.Ⅱ为盐酸稀释时的pH值变化曲线
B.b点酸的总浓度大于a点酸的总浓度
C.a点Kw的数值比c点Kw的数值大
D.b点溶液的导电性比c点溶液的导电性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧燃料电池是一种新型的化学电源,其构造如图一所示:a、b两个电极均由多孔碳制成,通入的气体由孔隙中逸出,并在电极表面放电。

(1)a电极反应式是_______________________;
(2)该燃料电池生成了360 kg的水,则电路中通过了_____________mol的电子。
(3)用如图二所示电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极反应式是___________________。
②Y电极的材料是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)依据氧化还原反应2Ag+(ag)+Cu(s)==Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:

电极X的材料是_______;电解质溶液Y是_________________;银电极为电池的________极,发生的电极反应为______________________;X电极上发生的电极反应为______________________。
(2)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入CH4和O2,该电池即为氢氧燃料电池,

写出A电极反应式:___________________________________;写出B电极反应式:_______________________;写出该电池反应:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A. 把煤隔绝空气加强热使之分解的过程叫干馏
B. 煤的干馏包含着物理变化和化学变化
C. 煤中含有大量苯和甲苯,可以用先干馏后分馏的方法将其分离开
D. 以煤为主要原料,可以合成甲醇等液体燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(分子式为N2H4,又称联氨)具有可燃性,在氧气中完全燃烧生成氮气,可用作燃料电池的燃料。由题图信息可知下列叙述不正确的是( )

甲 乙
A. 甲为原电池,乙为电解池
B. b电极的电极反应式为O2+4e-=2O2-
C. d电极的电极反应式为Cu2++2e-=Cu
D. c电极质量变化128 g时,理论消耗标准状况下的空气约为112 L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com