
 ij����С����������װ��Ѹ���Ʊ������������ṩ���Լ��У�Ũ���ᡢ����ʳ��ˮ������������Һ��������ع��壮��2KMnO4+16HCl��Ũ���T2KCl+2MnCl2+5Cl2��+8H2O���Իش�
ij����С����������װ��Ѹ���Ʊ������������ṩ���Լ��У�Ũ���ᡢ����ʳ��ˮ������������Һ��������ع��壮��2KMnO4+16HCl��Ũ���T2KCl+2MnCl2+5Cl2��+8H2O���Իش�


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���÷�Ӧ��Fe3+�������� |
| B���÷�Ӧ��Cu�������� |
| C��2mol Fe3+��Ӧ�õ�4NA������ |
| D�����������뻹ԭ��������ʵ���֮��Ϊ1��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
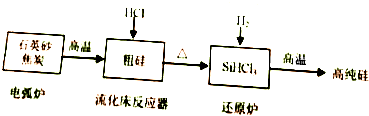 ���ڵؿ��еĺ����ϸߣ��輰�仯����Ŀ��������Ѿã����ִ��������й㷺Ӧ�ã��ش��������⣺
���ڵؿ��еĺ����ϸߣ��輰�仯����Ŀ��������Ѿã����ִ��������й㷺Ӧ�ã��ش��������⣺| ���� | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
| �е�/�� | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| m-n | 0 | 1 | 2 | 3 |
| ������ǿ�� | �� �� | �� ǿ | ǿ | �� ǿ |
| ʵ �� | HClO | H3PO4 | HNO3 | HClO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
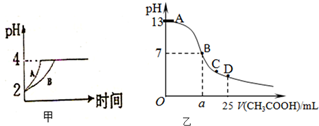 ��ѧѧ���е�ƽ��������Ҫ��������ѧƽ�⡢����ƽ�⡢ˮ��ƽ����ܽ�ƽ�����֣��Ҿ�������������ԭ������ش��������⣺
��ѧѧ���е�ƽ��������Ҫ��������ѧƽ�⡢����ƽ�⡢ˮ��ƽ����ܽ�ƽ�����֣��Ҿ�������������ԭ������ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ʳƷ����Ĥ�ɷ�Ϊ������ϩ |
| B����ȩ����Ϊ����Ʒ�ķ����� |
| C���������ᴿ�����ʲ��������������� |
| D��ҽ�������������ľƾ����������Ϊ95% |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com