
| T/�� | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
���� ��1����ѧƽ�ⳣ������ָ��һ���¶��£����淴Ӧ�ﵽƽ��ʱ��������Ũ�ȵĻ�ѧ���������ݵij˻����Ը���Ӧ��Ũ�ȵĻ�ѧ���������ݵij˻����õı�ֵ���ݴ���д��
��2���ɱ������ݿ�֪���¶�Խ��ѧƽ�ⳣ��Խ�������¶�ƽ��������Ӧ�ƶ�������Ӧ�����ȷ�Ӧ�������¶ȣ���Ӧ��������
��3����С������Ũ�ȣ�ƽ��������Ӧ�����ƶ���ƽ�ⳣ��ֻ���¶�Ӱ�죻
��4�������ʱ��Ũ����Qc����ƽ�ⳣ���Ƚ��жϷ�Ӧ���з��ݴ˽��
��5������CO2��ת���ʣ���������ʽ��ʾ��ƽ��ʱ����ֵ����ʵ������÷�Ӧ�������������ķ�Ӧ�������ʵ�������Ũ�ȴ���ƽ�ⳣ������ʽ���Լ����ƽ�ⳣ��������ʼʱͶ��3.6mol CO��3.6mol H2O��1.8mol H2ʱ����ת����CO��Ũ��Ϊxmol/L������ƽ�ⳣ���ɼ����x��ֵ����ȷ��H2��ƽ��Ũ�ȣ��ݴ˽��
��� �⣺��1�����淴ӦCO2��g��+H2��g��?CO��g��+H2O��g���Ļ�ѧƽ�ⳣ������ʽk=$\frac{c��CO��•c��H{\;}_{2}O��}{c��CO{\;}_{2}��•c��H{\;}_{2}��}$��
�ʴ�Ϊ��$\frac{c��CO��•c��H{\;}_{2}O��}{c��CO{\;}_{2}��•c��H{\;}_{2}��}$��
��2���ɱ������ݿ�֪���¶�Խ��ѧƽ�ⳣ��Խ�������¶�ƽ��������Ӧ�ƶ�������Ӧ�����ȷ�Ӧ�������¶ȣ����淴Ӧ���ʶ�����
�ʴ�Ϊ�����ȣ�����
��3����С������Ũ�ȣ�ƽ��������Ӧ�����ƶ���ƽ�ⳣ��ֻ���¶�Ӱ�죬���Լ�СCO��Ũ�ȣ�ƽ�ⳣ�����䣬
�ʴ�Ϊ������Ӧ�����䣻
��4����ʱ��Ũ����Qc=$\frac{1��3}{1��5}$=0.6��С��ƽ�ⳣ��0.9���ʷ�Ӧ������Ӧ���У���H2O���������ʱ���������С��
�ʴ�Ϊ��С��
��5�������з���4mol CO2��6mol H2��CO2��H2��Ũ�ȷֱ�Ϊ2mol/L��3mol/L����
CO2��g��+H2��g��?CO��g��+H2O��g��
��ʼ��mol/L����2 3 0 0
�仯��mol/L����1.2 1.2 1.2 1.2
ƽ�⣨mol/L����0.8 1.8 1.2 1.2
��CO���������Ϊ$\frac{1.2}{5}$��100%=24%��K=$\frac{1.2��1.2}{0.8��1.8}$=1�����Դ�ʱ���¶�Ϊ830�棬
����ʼʱͶ��3.6mol CO��3.6mol H2O��1.8mol H2ʱ����Ũ�ȷֱ�Ϊ2��1.8mol/L��1.8mol/L��0.9mol/L����ת����CO��Ũ��Ϊxmol/L����
CO2��g��+H2��g��?CO��g��+H2O��g��
��ʼ��mol/L����0 0.9 1.8 1.8
�仯��mol/L����x x x x
ƽ�⣨mol/L����x 0.9+x 1.8-x 1.8-x
K=$\frac{��1.8-x����1.8-x��}{x��0.9+x��}$=1������x=0.72������CO���������Ϊ$\frac{1.8-0.72}{0.9+1.8+1.8}$��100%=24%��H2��ƽ��Ũ��Ϊ��0.9+0.72��mol/L=1.62mol/L��
�ʴ�Ϊ��24%��830�棻24%��1.62mol/L��
���� ���⿼�黯ѧƽ�ⳣ����ƽ�ⳣ����Ӧ�õȣ��Ѷ��еȣ�ע�����ջ�ѧƽ�ⳣ������;��1���жϷ�Ӧ���еij̶ȣ�2���жϷ�Ӧ����ЧӦ��3���жϷ�Ӧ���еķ���4������ת���ʵȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe2O3��������������� | B�� | Al2O3�������ͻ���� | ||
| C�� | ��ˮ���Ե�̲��� | D�� | �����������������ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
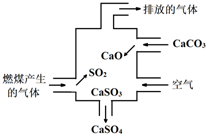
| A�� | ʹ�ô�װ�ÿɼ��ٵ�������������γ� | |
| B�� | �����Ը��������Һ������������Ƿ��� | |
| C�� | �������̵��ܷ�Ӧ�ɱ�ʾΪ��2SO2+2CaCO3+O2=2CaSO4+2CO2 | |
| D�� | �ŷŵ������Ǵ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
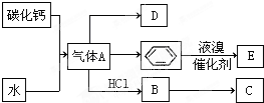
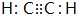 ��D�Ŀռ乹��Ϊƽ��ṹ������Ϊ120�㣻
��D�Ŀռ乹��Ϊƽ��ṹ������Ϊ120�㣻 +Br2 $\stackrel{FeBr_{3}}{��}$
+Br2 $\stackrel{FeBr_{3}}{��}$ +HBr���䷴Ӧ����Ϊȡ����Ӧ��
+HBr���䷴Ӧ����Ϊȡ����Ӧ��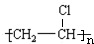 ���䷴Ӧ����Ϊ�Ӿ۷�Ӧ��
���䷴Ӧ����Ϊ�Ӿ۷�Ӧ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na+��Cu2+��NO3-��CO32- | B�� | NH4+��K+��SO42-��HCO3- | ||
| C�� | Mg2+��NH4+��SO42-��Cl- | D�� | Fe2+��Na+��SO42-��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
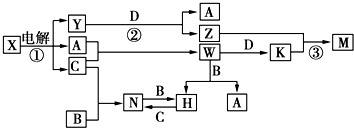
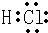 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ʱ��t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
| ��ѹǿp/100kPa | 4.91 | 5.58 | 6.32 | 7.31 | 8.54 | 9.50 | 9.52 | 9.53 | 9.53 |
| A�� | ��Ӧ��ǰ��Сʱ��ƽ������Ϊv��A���T0.0122mol•L-1•h-1 | |
| B�� | ���������䣬���£����淴Ӧ���ʶ����� | |
| C�� | �÷�Ӧ����ƽ��ʱA��ת����Ϊ94.1% | |
| D�� | ���ݻ��������С��ԭ����һ�룬��ƽ���C�İٷֺ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ۼ���ϡ�����У�2Fe+6H+�TFe3++3H2�� | |
| B�� | �������������������Fe3O4+8H+�T3Fe3++4H2O | |
| C�� | ���Ȼ�������Һ��ϡ�����ϣ�3Fe2++4H++NO3-�T3Fe3++2H2O+NO�� | |
| D�� | ����м����Fe3+��Һ�У�Fe3++Fe�T2Fe2+ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com