
【题目】五种短周期元素A、B、C、D、E原子序数依次增大,结合下列信息:A原子核外电子总数是内层电子数的三倍,A、E同主族;B的最高价氧化物对应的水化物F与其气态氢化物G反应,得到离子化合物H;C的焰色应呈黄色;D在同周期中形成的简单离子,其离子半径最小;
回答下列问题:
(1)写出D在元素周期表中的位置:______________。
(2)化合物H的水溶液pH_______7(填“大于”、“等于”“小于”),其原因是______________用离子方程式表示。
(3)上述元素的最高价氧化物对应水化物中,有一种物质在一定条件下均能与其他四种物质发生化学反应,写出该物质的电子式:_______。
(4)请设计实验证明A、B、E的非金属性强弱关系:________。
【答案】 第三周期、 第IIIA族 小于 NH4++H2O![]() NH3·H2O+H+
NH3·H2O+H+ ![]() 将过量的稀硝酸加入到碳酸钠溶液中,观察到气泡,再将生成的二氧化碳除去挥发出的HNO3通入到硅酸钠溶液,观察到有白色沉淀生成,证明非金属性N>C>Si
将过量的稀硝酸加入到碳酸钠溶液中,观察到气泡,再将生成的二氧化碳除去挥发出的HNO3通入到硅酸钠溶液,观察到有白色沉淀生成,证明非金属性N>C>Si
【解析】由已知A、B、C、D、E为原子序数依次增大的短周期元素,A原子核外电子总数是内层电子数的三倍,则A为碳元素;A、E同主族,则E为硅元素;B的最高价氧化物对应的水化物F与其气态氢化物G反应,得到离子化合物H,则B为氮元素、F为硝酸、G为氨气、H为硝酸铵;C的焰色应呈黄色,则C为钠元素;D在同周期中形成的简单离子,离子半径最小,且原子序数大于钠,则D为铝元素。
(1)D为铝元素,在元素周期表中处于第三周期第ⅢA族。
(2)化合物H为硝酸铵,属于强酸弱碱盐,由于铵根离子水解,使其水溶液呈酸性,所以pH<7,用离子方程式表示为NH4++H2O![]() NH3·H2O+H+。
NH3·H2O+H+。
(3)A、B、C、D、E的最高价氧化物对应水化物分别为:碳酸、硝酸、氢氧化钠、氢氧化铝、硅酸,其中氢氧化钠在一定条件下均能与其他四种物质发生化学反应,其的电子式为:![]() 。
。
(4)元素的非金属性越强,对应的最高价含氧酸的酸性越强,根据强酸制弱酸原理设计实验,将过量的稀硝酸加入到碳酸钠溶液中,观察到气泡,再将生成的二氧化碳除去挥发出的HNO3然后通入到硅酸钠溶液中,观察到有白色沉淀生成,则证明非金属性N>C>Si。


 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
【题目】如图所示,ΔH1=-393.5kJ·mol-1,ΔH2=-395.4kJ·mol-1,

下列说法或表示式正确的是
A. 石墨和金刚石的转化是物理变化
B. C(s、石墨)===C(s、金刚石)ΔH =+1.9kJ·mol-1
C. 金刚石的稳定性强于石墨
D. 断裂1mol石墨的化学键吸收的能量比断裂1mol金刚石的化学键吸收的能量少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解足量下列溶液一段时间后,再加入一定量括号内的纯净物,能使溶液恢复到原来的成分和浓度的是
A. AgNO3[AgNO3] B. NaOH[NaOH] C. KCl[H2O] D. CuSO4[CuO]
【答案】D
【解析】石墨电极为惰性电极,溶液中阳离子在阴极放电,阴离子在阳极放电。A、电解AgNO3溶液,Ag+在阴极放电生成Ag,OH-在阳极放电生成O2,且n(Ag)∶n(O2)=2∶1,则应加入Ag2O恢复浓度,故A错误;B、电解NaOH溶液,H+在阴极放电生成H2,OH-在阳极放电生成O2,且n(H2)∶n(O2)=2∶1,则应加入一定量的H2O恢复原样,故B错误;C、电解KCl溶液,H+在阴极放电生成H2,Cl-在阳极放电生成Cl2,且n(H2)∶n(Cl2)=1∶1,则应加入一定量HCl恢复原样,故C错误;D、电解CuSO4溶液,Cu2+在阴极放电生成Cu,OH-在阳极放电生成O2,且n(Cu)∶n(O2)=2∶1,则应加入一定量CuO恢复原样,故D正确。故选D。
点睛:分析电解反应的原理,在两极析出什么物质(固体或气体),相当于什么物质脱离反应体系,根据元素守恒和原子比例,加入对应的物质,即可使溶液完全复原。
【题型】单选题
【结束】
28
【题目】工业上用电解法处理含镍酸性废水并得到单质Ni的原理如图所示。下列说法不正确的是

已知:①Ni2+在弱酸性溶液中发生水解
②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)
A. 碳棒上发生的电极反应:4OH--4e-=O2↑+2H2O
B. 电解过程中,B中NaCl溶液的物质的量浓度将不断减少
C. 为了提高Ni的产率,电解过程中需要控制废水pH
D. 若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释实验事实的离子方程式正确的是
A. 实验室制取Cl2时,用NaOH溶液吸收尾气:Cl2 + 2OH- =ClO-+ Cl-+H2O
B. 向FeCl3溶液中加入Fe粉,溶液变为浅绿色:Fe3+ + Fe =2Fe2+
C. 铜片放入稀HNO3中生成气体:Cu + 4H+ +2NO![]() =Cu2+ + 2NO2↑+2H2O
=Cu2+ + 2NO2↑+2H2O
D. Ba(OH)2溶液与稀H2SO4反应生成白色沉淀:Ba2+ + SO42- + H+ +OH- =BaSO4↓ + H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
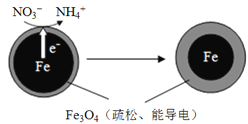
【题目】生活污水和某些工业废水中的含氮化合物经转化最终会以硝酸盐的形式进入水体,若大量排放会造成水体富营养化。用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一。Fe还原水体中NO3-的反应原理如右图所示。
(1)下列说法属于水体污染的危害的有______(填字母)。
a.加剧水资源短缺 b.危害人体健康
(2)NO3-中氮元素的化合价为______。
(3)Fe在反应过程中发生的是______(选填“氧化”或“还原”)反应。
(4)将足量铁粉投入某水体样本中,经一段时间后,测得溶液中离子浓度的有关数据如下(其他离子忽略不计)。
离子 | Na+ | H+ | NO3 | NH4+ | Fe2+ |
浓度/(mol·L1) | 5.0×102 | 5.0×102 | 6.4×101 | y | 2.4×101 |
表中y =______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关AgCl沉淀的溶解平衡的说法中正确的是( )
A.AgCl沉淀生成和沉淀溶解不断进行,但速率相等
B.AgCl难溶于水,溶液中没有Ag+和Cl-
C.升高温度,AgCl沉淀的溶解度减小
D.在有AgCl沉淀生成的溶液中加入NaCl固体,AgCl沉淀溶解的量不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com