
| A. | Na,Mg,Al | B. | N,O,F | C. | Li,Na,K | D. | I,Br,Cl |
 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
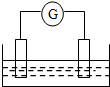 如图是常见原电池装置,电流表G发生偏转:
如图是常见原电池装置,电流表G发生偏转:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铝溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| B. | Cu溶于稀硝酸HNO3:Cu+2H++NO3-═Cu2++NO2↑+H2O | |
| C. | Fe2(SO4)3溶液和Ba(OH)2溶液反应:Fe3++SO42-+Ba2++3OH-═Fe(OH)3↓+BaSO4↓ | |
| D. | 向Fe(OH)3中加入氢碘酸:Fe(OH)3+3H+═Fe3++3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在元素周期表金属与非金属分界线附近能找到制半导体材料的元素 | |
| B. | 离子键、共价键、氢键都是化学键 | |
| C. | 元素周期律是元素原子核外电子排布周期性变化的必然结果 | |
| D. | 元素周期表揭示了化学元素间的内在联系,是化学发展史上的重要里程碑 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 将下列物质分别装入有水的锥形瓶里,立即塞紧带U形管的塞子,发现U形管内滴有红墨水的水面呈现如图所示状态.加入的物质不可能是(不考虑加入物质引起的溶液体积的变化)( )
将下列物质分别装入有水的锥形瓶里,立即塞紧带U形管的塞子,发现U形管内滴有红墨水的水面呈现如图所示状态.加入的物质不可能是(不考虑加入物质引起的溶液体积的变化)( )| A. | 固体NaOH | B. | 浓H2SO4 | ||
| C. | Ba(OH)2•8H2O与NH4Cl糊状物 | D. | CaO固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用可再生资源、用超临界二氧化碳替代有机溶液剂、注重原子的经济性、采用低能耗生产工艺等都是绿色化学的内容 | |
| B. | 煤的干馏得到的煤焦油中可以分离出苯及其同系物,也可以分离出乙烯、丙烯等石油化工原料 | |
| C. | 用原子吸收光谱可以确定物质中含有哪些金属元素 | |
| D. | 淀粉、麦芽糖糖水解后的最终产物都是葡萄糖 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com