
”¾ĢāÄæ”æĻĀĮŠ¶Ō»Æѧ·“Ó¦·½ĻņµÄĖµ·Ø£¬ÕżČ·µÄŹĒ
A.Ķ¬Ņ»ĪļÖŹµÄ¹Ģ”¢Ņŗ”¢ĘųČżÖÖדĢ¬µÄģŲÖµµŻ¼õ
B.³£ĪĀĻĀ·“Ó¦2Na2SO3(s)+O2(g)=2Na2SO4(s£©ÄÜ×Ō·¢½ųŠŠ£¬Ōņ”÷H<0
C.CaCO3(s)=CaO(s)+CO2(g£©”÷H>0£¬”÷S>0£¬²»ĀŪŌŚŗĪÖÖĢõ¼žĻĀ¶¼²»æÉÄÜ×Ō·¢
D.ŅņĪŖģŹ±äŗĶģŲ±ä¶¼Óė·“Ó¦µÄ×Ō·¢ŠŌÓŠ¹Ų£¬Ņņ“ĖģŹ±ä»ņÉŹ±ä¾łæÉŅŌµ„¶Ą×öĪŖÅŠ¶Ļ·“Ó¦ÄÜ·ń×Ō·¢½ųŠŠµÄÅŠ¾Ż
”¾“š°ø”æB
”¾½āĪö”æ
A. Ķ¬Ņ»ĪļÖŹµÄ¹Ģ”¢Ņŗ”¢ĘųČżÖÖדĢ¬µÄģŲÖµµŻŌö£¬AĻī“ķĪó£»
B. ³£ĪĀĻĀ·“Ó¦2Na2SO3(s)+O2(g)=2Na2SO4(s) ”÷S£¼0£¬ÄÜ×Ō·¢½ųŠŠÖ÷ŅŖŹĒŅņĪŖ”÷H<0£¬BĻīÕżČ·£»
C. CaCO3(s)=CaO(s)+CO2(g£©”÷H>0£¬”÷S>0£¬øł¾Ż×ŌÓÉÄÜÅŠ¾ŻæÉÖŖ£¬Čō×Ō·¢½ųŠŠ£¬Ōņ![]() £¬¼“øßĪĀĻĀæÉ×Ō·¢½ųŠŠ£¬CĻī“ķĪó£»
£¬¼“øßĪĀĻĀæÉ×Ō·¢½ųŠŠ£¬CĻī“ķĪó£»
D. ģŹ±äŗĶģŲ±ä¶¼Óė·“Ó¦µÄ×Ō·¢ŠŌÓŠ¹Ų£¬µ«ģŹ±ä»ņÉŹ±äµ„¶Ą×öĪŖÅŠ¶Ļ·“Ó¦ÄÜ·ń×Ō·¢½ųŠŠµÄÅŠ¾ŻŹĒʬĆęµÄ£¬Ó¦øĆÓĆø“ŗĻÅŠ¾Ż£¬¼“![]() Ą“×ŪŗĻÅŠ¶Ļ£¬DĻī“ķĪó£»
Ą“×ŪŗĻÅŠ¶Ļ£¬DĻī“ķĪó£»
“š°øŃ”B”£
»Æѧ·“Ó¦ÄÜ·ń×Ō·¢½ųŠŠ£¬Č”¾öÓŚģŹ±äŗĶģŲ±äµÄ×ŪŗĻÅŠ¾Ż£¬µ±![]() Ź±£¬·“Ó¦æÉ×Ō·¢½ųŠŠ”£
Ź±£¬·“Ó¦æÉ×Ō·¢½ųŠŠ”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”湤ŅµÉĻÉś²śøõµ„ÖŹÉę¼°µÄ·“Ó¦ČēĻĀ£ŗ
Na2Cr2O7£«2C![]() Cr2O3£«Na2CO3£«CO”ü
Cr2O3£«Na2CO3£«CO”ü
Cr2O3£«2Al![]() 2Cr£«Al2O3
2Cr£«Al2O3
(1) Cr»łĢ¬Ō×ÓµÄŗĖĶāµē×ÓÅŲ¼Ź½ĪŖ________”£

(2) Na”¢O”¢CµÄµŚŅ»µēĄėÄܓӓ󵽊”µÄĖ³ŠņĪŖ________”£
(3) ÓėCO![]() »„ĪŖµČµē×ÓĢåµÄŅ»ÖÖ·Ö×ÓĪŖ________(Ģī»ÆѧŹ½)”£
»„ĪŖµČµē×ÓĢåµÄŅ»ÖÖ·Ö×ÓĪŖ________(Ģī»ÆѧŹ½)”£
(4) Cr2O3¾ßÓŠĮ½ŠŌ£¬ČÜÓŚNaOHČÜŅŗŠĪ³ÉÅäŗĻĪļNa[Cr(OH)4]”£
Na[Cr(OH)4]ÖŠÅäĢåµÄ»ÆѧŹ½ĪŖ____________£¬1 moløĆÅäŗĻĪļÖŠŗ¬¦Ņ¼üŹżÄæĪŖ_________”£
(5) ŗĻ½šCrAl¾§ĢåµÄ¾§°ūČēÓŅĶ¼ĖłŹ¾£¬Š“³öøĆŗĻ½šµÄ»ÆѧŹ½£ŗ________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŽ»ś·Ē½šŹō²ÄĮĻ”¢½šŹō²ÄĮĻŗĶÓŠ»śøß·Ö×Ó²ÄĮĻ²¢³ĘĪŖČż“ó²ÄĮĻ£¬ŹĒ·¢Õ¹øߊĀ¼¼ŹõµÄ»łŹÆ£¬ŌŚĪ“Ą“æĘ¼¼·¢Õ¹ÖŠ·¢»Ó×ÅÖŲŅŖµÄ×÷ÓĆ”£
£Ø1£©NieriteŹĒŅ»ÖÖøßČŪµćøßÓ²¶ČµÄĢՓɲÄĮĻ”£NieriteµÄĦ¶ūÖŹĮæĪŖ140 g/mol£¬ĘäÖŠ¹čŌŖĖŲµÄÖŹĮæ·ÖŹżĪŖ60%”£ŅŃÖŖ1 mol NH3Óė×ćĮæµÄSiCl4³ä·Ö·“Ó¦ŗóæɵƵ½35 g NieriteÓė3 mol HClĘųĢ唣NieriteµÄ»ÆѧŹ½ĪŖ___________”£
£Ø2£©K½šŹĒ³£¼ūµÄ¹ó½šŹō²ÄĮĻ£¬³ż»Ę½šĶā£¬»¹ŗ¬ÓŠŅų”¢ĶÖŠµÄŅ»ÖÖ»ņĮ½ÖÖ½šŹō”£ĪŖ²ā¶Øij18K½šŃłĘ·µÄ×é³É£¬½«2£®832 gѳʷ·ŪĖéŗóĶ¶Čė×ćĮæµÄÅØĻõĖįÖŠ£¬¹ĢĢåČ«²æČܽāŗó£¬ŹÕ¼Æµ½NO2ŗĶN2O4µÄ»ģŗĻĘųĢå224 mL£ØÕŪĖćÖĮ±ź×¼×“æö£¬ĻĀĶ¬£©£¬½«øĆ»ģŗĻĘųĢåÓė84 mL O2»ģŗĻŗó»ŗ»ŗĶØČėĖ®ÖŠ£¬Ē”ŗƱ»ĶźČ«ĪüŹÕ”£
ĢīŠ“øĆ18K½šµÄ³É·Ö±ķ£Ø¾«Č·ÖĮ0£®01%£¬Čō²»ŗ¬øĆ½šŹōŌņĢī0£©”£
18K½š³É·Ö | Au | Ag |
ŗ¬Įæ£ØÖŹĮæ·ÖŹż£© | 75£®00% | _________ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æI£®·“Ó¦![]() Fe2O3£Øs£©+CO£Øg£©
Fe2O3£Øs£©+CO£Øg£©![]() Fe£Øs£©+CO2£Øg£©H<0£¬ŌŚ1000”ęµÄĘ½ŗā³£ŹżµČÓŚ4.0£®ŌŚŅ»øöČŻ»żĪŖ10LµÄĆܱÕČŻĘ÷ÖŠ£¬1000”ꏱ¼ÓČėFe”¢Fe2O3”¢CO”¢CO2ø÷1.0mol£¬·“Ó¦¾¹ż10minŗó“ļµ½Ę½ŗā£®
Fe£Øs£©+CO2£Øg£©H<0£¬ŌŚ1000”ęµÄĘ½ŗā³£ŹżµČÓŚ4.0£®ŌŚŅ»øöČŻ»żĪŖ10LµÄĆܱÕČŻĘ÷ÖŠ£¬1000”ꏱ¼ÓČėFe”¢Fe2O3”¢CO”¢CO2ø÷1.0mol£¬·“Ó¦¾¹ż10minŗó“ļµ½Ę½ŗā£®
£Ø1£©COµÄĘ½ŗā×Ŗ»ÆĀŹ= ______ ”£
£Ø2£©ÓūĢįøßCOµÄĘ½ŗā×Ŗ»ÆĀŹ£¬“Ł½ųFe2O3µÄ×Ŗ»Æ£¬æɲÉČ”µÄ“ėŹ©ŹĒ ______
a£®Ģįøß·“Ó¦ĪĀ¶Č b£®Ōö“ó·“Ó¦ĢåĻµµÄŃ¹Ēæ
c£®Ń”Č”ŗĻŹŹµÄ“߻ƼĮ d£®¼°Ź±ĪüŹÕ»ņŅĘ³ö²æ·ÖCO2
e£®·ŪĖéæóŹÆ£¬Ź¹ĘäÓėĘ½ŗā»ģŗĻĘųĢå³ä·Ö½Ó“„
II£®£Ø1£©øßĀÆĮ¶Ģś²śÉśµÄ·ĻĘųÖŠµÄCOæɽųŠŠ»ŲŹÕ£¬Ź¹ĘäŌŚŅ»¶ØĢõ¼žĻĀŗĶH2·“Ó¦Öʱø¼×“¼£ŗ CO£Øg£©+2H2£Øg£©CH3OH£Øg£©”£Ēėøł¾ŻĶ¼Ź¾»Ų“šĻĀĮŠĪŹĢā£ŗ
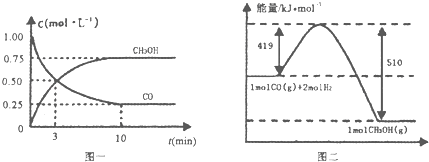
£Ø1£©“Ó·“Ó¦æŖŹ¼µ½Ę½ŗā£¬ÓĆH2ÅØ¶Č±ä»Æ±ķŹ¾Ę½¾ł·“Ó¦ĖŁĀŹv£ØH2£©= ______ ”£
£Ø2£©ČōŌŚĪĀ¶ČŗĶČŻ»żĻąĶ¬µÄČżøöĆܱÕČŻĘ÷ÖŠ£¬°“²»Ķ¬·½Ź½Ķ¶Čė·“Ó¦Īļ£¬²āµĆ·“Ó¦“ļµ½Ę½ŗā ¼µÄÓŠ¹ŲŹż¾ŻČēĻĀ±ķ£ŗ
ČŻĘ÷ | ·“Ó¦ĪļĶ¶ČėµÄĮæ | ·“Ó¦ĪļµÄ×Ŗ»ÆĀŹ | CH3OHµÄÅØ¶Č | ÄÜĮæ±ä»Æ £ØQ1£¬Q2£¬Q3¾ł“óÓŚ0£© |
¼× | 1molCOŗĶ2molH2 | a1 | c1 | ·Å³öQ1kJČČĮæ |
ŅŅ | 1molCH3OH | a2 | c2 | ĪüŹÕQ2kJČČĮæ |
±ū | 2molCOŗĶ4molH2 | a3 | c3 | ·Å³öQ3kJČČĮæ |
ŌņĻĀĮŠ¹ŲĻµÕżČ·µÄŹĒ ______ £®
A c1=c2 B 2Q1=Q3 C 2a1=a3 D a1+a2=1 E øĆ·“Ó¦ČōÉś³É1molCH3OH£¬Ōņ·Å³ö£ØQ1+Q2£©kJČČĮ攣
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æNAŹĒ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A.16.25g FeCl3Ė®½āŠĪ³ÉµÄFe(OH)3½ŗĢåĮ£×ÓŹżĪŖ0.1NA
B.92.0g øŹÓĶ(±ūČż“¼)ÖŠŗ¬ÓŠōĒ»łŹżĪŖ1.0NA
C.22.4L(±ź×¼×“æö)ė²Ęųŗ¬ÓŠµÄÖŹ×ÓŹżĪŖ18NA
D.1.0mol CH4ÓėCl2ŌŚ¹āÕÕĻĀ·“Ӧɜ³ÉµÄCH3Cl·Ö×ÓŹżĪŖ1.0NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼ŹĒ֊ѧ»ÆѧŹµŃéÖŠ³£¼ūµÄÖʱøĘųĢå²¢½ųŠŠÄ³Š©ĪļÖŹµÄ¼ģŃéŗĶŠŌÖŹŹµŃéµÄ×°ÖĆ£¬AŹĒÖʱøĘųĢåµÄ×°ÖĆ£¬C”¢D”¢E”¢FÖŠŹ¢×°µÄŅŗĢåæÉÄÜĻąĶ¬£¬Ņ²æÉÄܲ»Ķ¬”£ŹŌ»Ų“š£ŗ
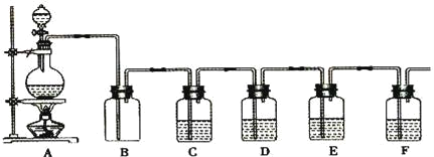
£Ø1£©Čē¹ūAÖŠµÄ¹ĢĢåĪļÖŹŹĒĢ¼£¬·ÖŅŗĀ©¶·ÖŠŹ¢×°µÄŹĒÅØĮņĖį£¬ŹŌŠ“³ö·¢ÉśµÄ»Æѧ·“Ó¦·½³ĢŹ½£ŗ____£¬ČōŅŖ¼ģŃéÉś³ÉµÄ²śĪļ£¬ŌņB”¢C”¢D”¢E”¢FÖŠÓ¦·Ö±š¼ÓČėµÄŹŌ¼ĮĪŖ__”¢__”¢__”¢__”¢__£¬EÖŠŹŌ¼ĮŗĶCÖŠĻąĶ¬£¬EÖŠŹŌ¼ĮĖłĘšµÄ×÷ÓĆ__£¬B×°ÖĆ³żæɼģ³öij²śĪļĶā£¬»¹æÉĘšµ½__×÷ÓĆ”£
£Ø2£©Čō½ųŠŠÉĻŹöŹµŃ鏱ŌŚFÖŠµĆµ½10.0 g¹ĢĢ壬ŌņAÖŠ·¢Éś·“Ó¦×ŖŅʵĵē×ÓŹżĪŖ__øö”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
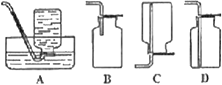
”¾ĢāÄæ”æČēĶ¼ĪŖŹµŃéŹŅÖʱøŅŅČ²²¢½ųŠŠŠŌÖŹŃéÖ¤µÄ×°ÖĆ(¼Š³ÖŅĒĘ÷¼ŗĀŌČ„)”£

£Ø1£©ŹµŃéæŖŹ¼Ē°£¬Ź×ĻČ½ųŠŠµÄ²Ł×÷ŹĒ___£»
£Ø2£©ŹµŃéŹŅÖĘø÷ŅŅČ²µÄ·½³ĢŹ½ĪŖ___£»
£Ø3£©ŅĒĘ÷AŌŚ°²×°Ē°±ŲŠė½ųŠŠµÄ²Ł×÷ŹĒ___£¬ĪŖ·ĄÖ¹ĘųĢåÉś³ÉµÄĖŁĀŹ¹żæģ£¬ÓÉAµĪČėBµÄŹŌ¼ĮĪŖ___”£
£Ø4£©×°ÖĆCæÉŃ”ÓƵďŌ¼ĮĪŖ___(Š“³öŅ»ÖÖ¼“æÉ)£¬Ęä×÷ÓĆĪŖ___£»
£Ø5£©·“Ó¦æŖŹ¼ŗó£¬DÖŠµÄĻÖĻóĪŖ___£¬Ėł·¢Éś·“Ó¦µÄ·“Ó¦ĄąŠĶĪŖ___£»
£Ø6£©DÖŠŃéÖ¤ŹµŃé½įŹųŗó”£BÖŠ·“Ó¦ČŌŌŚ¼ĢŠų”£“ĖŹ±æɳ·Č„×°ÖĆD£¬ŌŚ×°ÖĆCÖ®ŗóĮ¬½ÓŹÕ¼Æ×°ÖĆ£¬ŅŌĻĀ×°ÖĆÖŠ×īŹŹŗĻÓĆÓŚŹÕ¼ÆŅŅČ²µÄŹĒ___”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æļŖ(Re)ŹĒČŪµćŗĶ·Šµć½ĻøߵĽšŹōµ„ÖŹÖ®Ņ»£¬ÓĆÓŚÖĘŌģøߊ§ÄÜÅēÉäŅżĒęŗĶ»š¼żŅżĒę”£“Ó»ŌīāæóŃõ»Æ±ŗÉÕŗóµÄŃĢµĄ»Ņ(Ö÷ŅŖ³É·ÖÓŠSiO2”¢Re2O7”¢MoO3”¢CuO”¢Fe3O4)ÖŠĢįČ”ļŖ·ŪµÄĮ÷³ĢČēĶ¼£ŗ
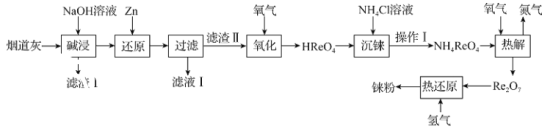
ŅŃÖŖ£ŗ
I.¹żļŖĖį(HReO4)ŹĒŅ×ČÜÓŚĖ®µÄŅ»ŌŖĒæĖį£¬µ«²»¾ßÓŠĒæŃõ»ÆŠŌ”£
II.¹żļŖĖįļ§(NH4ReO4)ŹĒ°×ɫʬד¾§Ģ壬Ī¢ČÜÓŚĄäĖ®£¬ČÜÓŚČČĖ®”£
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©”°¼ī½ž”±Ź±£¬Re2O7ŗĶMoO3ÓėNaOH·¢ÉśŅŌĻĀ·“Ó¦£ŗRe2O7+2NaOH=2NaReO4+H2O£»MoO3+2NaOH=Na2MoO4+H2O£¬Ōņ”°ĀĖŌüI”±µÄ³É·ÖĪŖ___”£
£Ø2£©¢Ł”°»¹Ō”±Ź±£¬Zn±»Ńõ»Æ³ÉZnO![]() £¬NaReO4±»»¹ŌÉś³ÉÄŃČܵÄ2ReO2”¤2H2O£¬øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ___”£
£¬NaReO4±»»¹ŌÉś³ÉÄŃČܵÄ2ReO2”¤2H2O£¬øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ___”£
¢Ś·Ö±šŌŚ20”ęŗĶ60”ęĢõ¼žĻĀ½ųŠŠ”°»¹Ō”±Ź±£¬ČÜŅŗÖŠReŗĶZnµÄŗ¬Įæ±ä»ÆČēĶ¼ÖŠĒśĻßĖłŹ¾£¬Čō²»æ¼ĀĒŹ±¼ä¶Ō»¹Ō·“Ó¦µÄÓ°Ļģ£¬”°»¹Ō”±Ź±£¬×īŗĆŃ”ŌńµÄĪĀ¶ČĪŖ___”£

£Ø3£©ĶØŃõĘų½ųŠŠ”°Ńõ»Æ”±Ź±£¬ĶłĶł½ųŠŠ¼ÓŃ¹£¬ÄæµÄŹĒ___”£”°Ńõ»Æ”±Ź±£¬ČōÉś³É376.5g¹żļŖĖį£¬ĄķĀŪÉĻĻūŗıź×¼×“æöĻĀŃõĘųµÄĢå»żĪŖ___ L”£
£Ø4£©”°³ĮļŖ”±Ź±£¬¼ÓČėČČNH4ClČÜŅŗÖĮ²śÉś°×É«³Įµķ£¬ĪŖŹ¹³Įµķ³ä·ÖĪö³ö²¢·ÖĄėµĆµ½“æ¾»NH4ReO4¾§Ģ壬”°²Ł×÷I”±°üĄØ___”¢Ļ“µÓ”¢øÉŌļ”£
£Ø5£©ĪŖĢįøßļŖµÄ“æ¶Č£¬”°¹żĀĖ”±µĆµ½µÄNH4ReO4Šč½ųŠŠĢį“棬Ģį“æĖłÓƵķ½·ØŹĒ___”£
£Ø6£©”°ČČ½ā”±Ź±£¬·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ___”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ(1)2017ÄźÖŠæĘŌŗÄ³ŃŠ¾æĶŶÓĶعżÉč¼ĘŅ»ÖÖŠĀŠĶNa-Fe3O4/HZSM-5¶ą¹¦ÄÜø“ŗĻ“߻ƼĮ£¬³É¹¦ŹµĻÖĮĖCO2Ö±½Ó¼ÓĒāÖĘČ”ŠĮĶéÖµĘūÓĶ£¬øĆŃŠ¾æ³É¹ū±»ĘĄ¼ŪĪŖ”°CO2“ß»Æ×Ŗ»ÆĮģÓņµÄĶ»ĘĘŠŌ½ųÕ¹”±”£
ŅŃÖŖ£ŗH2(g)+1/2O2(g)=H2O(l) ¦¤H1 = £aKJ/mol
C8H18(1)+25/2O2(g)=8CO2(g)+9H2O(1) ¦¤H2= £bKJ/mol
ŹŌŠ“³ö25”ę”¢101kPaĢõ¼žĻĀ£¬CO2ÓėH2·“Ӧɜ³ÉĘūÓĶ(ŅŌC8H18±ķŹ¾)µÄČČ»Æѧ·½³ĢŹ½_________________________________”£
(2)ĄūÓĆCO2¼°H2ĪŖŌĮĻ£¬ŌŚŗĻŹŹµÄ“߻ƼĮ(ČēCu/ZnO“߻ƼĮ)×÷ÓĆĻĀ£¬Ņ²æÉŗĻ³ÉCH3OH£¬Éę¼°µÄ·“Ó¦ÓŠ£ŗ
¼×£ŗCO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ”÷H= ”Ŗ 53.7kJ”¤mol-1 Ę½ŗā³£ŹżK1
CH3OH(g)+H2O(g) ”÷H= ”Ŗ 53.7kJ”¤mol-1 Ę½ŗā³£ŹżK1
ŅŅ£ŗCO2(g)+H2(g) ![]() CO(g)+H2O(g) ”÷H= + 41.2kJ”¤mol-1 Ę½ŗā³£ŹżK2
CO(g)+H2O(g) ”÷H= + 41.2kJ”¤mol-1 Ę½ŗā³£ŹżK2
¢ŁCO(g)+2H2(g) ![]() CH3OH(g)µÄĘ½ŗā³£ŹżK=______(ÓĆŗ¬K1”¢K2µÄ±ķ“ļŹ½±ķŹ¾)£¬øĆ·“Ó¦”÷H_____0(Ģī”°“óÓŚ”±»ņ”°Š”ÓŚ”±)”£
CH3OH(g)µÄĘ½ŗā³£ŹżK=______(ÓĆŗ¬K1”¢K2µÄ±ķ“ļŹ½±ķŹ¾)£¬øĆ·“Ó¦”÷H_____0(Ģī”°“óÓŚ”±»ņ”°Š”ÓŚ”±)”£
¢ŚĢįøßCO2×Ŗ»ÆĪŖCH3OHĘ½ŗā×Ŗ»ÆĀŹµÄ“ėŹ©ÓŠ___________(ĢīŠ“Į½Ļī)”£
¢Ū“߻ƼĮŗĶ·“Ó¦ĢåĻµµÄ¹ŲĻµ¾ĶĻńĖųŗĶŌæ³×µÄ¹ŲĻµŅ»Ńł£¬¾ßÓŠø߶ȵÄŃ”ŌńŠŌ”£ĻĀĮŠĖÄ×鏵Ń飬æŲÖĘCO2ŗĶH2³õŹ¼Ķ¶ĮĻ±Č¾łĪŖ1£ŗ2.2£¬¾¹żĻąĶ¬·“Ó¦Ź±¼ä(t1min)”£
ĪĀ¶Č(K) | “߻ƼĮ | CO2×Ŗ»ÆĀŹ(%) | ¼×“¼Ń”ŌńŠŌ(%) | ×ŪŗĻŃ”Ļī |
543 | Cu/ZnOÄÉĆ×°ō²ÄĮĻ | 12.3 | 42.3 | A |
543 | Cu/ZnOÄÉĆ×ʬ²ÄĮĻ | 11.9 | 72.7 | B |
553 | Cu/ZnOÄÉĆ×°ō²ÄĮĻ | 15.3 | 39.1 | C |
553 | Cu/ZnOÄÉĆ×ʬ²ÄĮĻ | 12.0 | 70.6 | D |
ÓɱķøńÖŠµÄŹż¾ŻæÉÖŖ£¬ĻąĶ¬ĪĀ¶ČĻĀ²»Ķ¬µÄ“߻ƼĮ¶ŌCO2µÄ×Ŗ»ÆĪŖCH3OHµÄŃ”ŌńŠŌÓŠĻŌÖųÓ°Ļģ£¬øł¾ŻÉĻ±ķĖłøųŹż¾Ż½įŗĻ·“Ó¦ŌĄķ£¬ĖłµĆ×īÓÅŃ”ĻīĪŖ___________(Ģī×ÖÄø·ūŗÅ)”£
(3)ŅŌCO”¢H2ĪŖŌĮĻŗĻ³É¼×“¼µÄ·“Ó¦ĪŖ£ŗCO(g)+2H2(g)![]() CH3OH(g)”£ŌŚĢå»ż¾łĪŖ2LµÄČżøöŗćČŻĆܱÕČŻĘ÷¢ń”¢¢ņ”¢¢óÖŠ£¬·Ö±š¶¼³äČė1molCOŗĶ2molH2£¬ČżøöČŻĘ÷µÄ·“Ó¦ĪĀ¶Č·Ö±šĪŖT1”¢T2”¢T3ĒŅŗć¶Ø²»±ä”£ĻĀĶ¼ĪŖČżøöČŻĘ÷ÖŠµÄ·“Ó¦¾ł½ųŠŠµ½5minŹ±H2µÄĢå»ż·ÖŹżŹ¾ŅāĶ¼£¬ĘäÖŠÓŠŅ»øöČŻĘ÷·“Ó¦Ņ»¶Ø“ļµ½Ę½ŗāדĢ¬”£
CH3OH(g)”£ŌŚĢå»ż¾łĪŖ2LµÄČżøöŗćČŻĆܱÕČŻĘ÷¢ń”¢¢ņ”¢¢óÖŠ£¬·Ö±š¶¼³äČė1molCOŗĶ2molH2£¬ČżøöČŻĘ÷µÄ·“Ó¦ĪĀ¶Č·Ö±šĪŖT1”¢T2”¢T3ĒŅŗć¶Ø²»±ä”£ĻĀĶ¼ĪŖČżøöČŻĘ÷ÖŠµÄ·“Ó¦¾ł½ųŠŠµ½5minŹ±H2µÄĢå»ż·ÖŹżŹ¾ŅāĶ¼£¬ĘäÖŠÓŠŅ»øöČŻĘ÷·“Ó¦Ņ»¶Ø“ļµ½Ę½ŗāדĢ¬”£
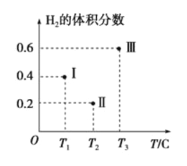
¢Ł0”«5minŹ±¼äÄŚČŻĘ÷¢ņÖŠÓĆCH3OH±ķŹ¾µÄ»Æѧ·“Ó¦ĖŁĀŹĪŖ_________________”£
¢ŚČżøöČŻĘ÷ÖŠŅ»¶Ø“ļµ½Ę½ŗāדĢ¬µÄŹĒČŻĘ÷________(ĢīŠ“ČŻĘ÷“śŗÅ)”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com