
在P+CuSO4+H2O—→Cu3P+H3PO4+H2SO4(未配平)的反应中,7.5 mol CuSO4可氧化P的物质的量为________mol。生成1 mol Cu3P时,参加反应的P的物质的量为________mol。
科目:高中化学 来源: 题型:
下列说法错误的是( )
A.用聚乙烯塑料代替聚乳酸塑料可减少白色污染(2014·天津理综,1B)
B.大量燃烧化石燃料是造成雾霾天气的一种重要因素(2014·天津理综,1C)
C.可燃冰主要是甲烷与水在低温高压下形成的水合物晶体,因此可存在于海底(2014·天津理综,3C)
D.乙烯可作水果的催熟剂(2014·四川理综,1A)
查看答案和解析>>
科目:高中化学 来源: 题型:
A~G是几种烃的分子球棍模型(如图),据此回答下列问题:
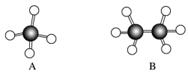
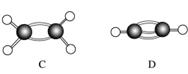

(1)常温下含碳量最高的气态烃是(填对应字母)__________________ ___________________________。
(2)能够发生加成反应的烃有(填数字)________种。
(3)一卤代物种类最多的是(填对应字母)________。
(4)写出实验室制取C的化学方程式_______________________________。
(5)写出F发生溴代反应的化学方程式______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)____ClO-+____Fe(OH)3+____===____Cl-+____FeO +____H2O
+____H2O
(2)____MnO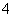 +____H2O2+____===____Mn2++____O2↑+____H2O
+____H2O2+____===____Mn2++____O2↑+____H2O
(3)某高温还原法制备新型陶瓷氮化铝(AlN)的反应体系中的物质有:Al2O3、C、N2、AlN、CO。
请将AlN之外的反应物与生成物分别填入以下空格内,并配平。
 +
+ +
+ —→
—→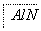 +
+
查看答案和解析>>
科目:高中化学 来源: 题型:
二氧化氯(ClO2)是一种高效、广谱、安全的杀菌消毒剂。
(1)氯化钠电解法是一种可靠的工业生产ClO2的方法。
①用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO 等杂质。除杂操作时,往粗盐水中先加入过量的________(填化学式),至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。经检测发现滤液中仍含有一定量的SO
等杂质。除杂操作时,往粗盐水中先加入过量的________(填化学式),至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。经检测发现滤液中仍含有一定量的SO ,其原因是________________________________________________________________________。
,其原因是________________________________________________________________________。
[已知:Ksp(BaSO4)=1.1×10-10,Ksp(BaCO3)=5.1×10-9]
②该法工艺原理如下图。其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2。

工艺中可以利用的单质有________(填化学式),发生器中生成ClO2的化学方程式为________________________________________________________________________。
(2)纤维素还原法制ClO2是一种新方法,其原理是:纤维素水解得到的最终产物D与NaClO3反应生成ClO2。完成反应的化学方程式:
 __(D)__+24NaClO3+12H2SO4===
__(D)__+24NaClO3+12H2SO4=== ClO2↑+
ClO2↑+ CO2↑+18H2O+
CO2↑+18H2O+ ________
________
(3)ClO2和Cl2均能将电镀废水中的CN-氧化为无毒的物质,自身被还原为Cl-。处理含CN-相同量的电镀废水,所需Cl2的物质的量是ClO2的________倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
①②(3)](2)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于化学镀银。
①H3PO2中,P元素的化合价为________。
②利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4∶1,则氧化产物为________(填化学式)。
(3)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。写出白磷与Ba(OH)2溶液反应的化学方程式________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
与Cl2相比较,ClO2处理水时被还原成Cl-,不生成有机氯代物等有害物质。工业上可用亚氯酸钠和稀盐酸为原料制备ClO2,反应如下:
NaClO2+HCl—→ClO2↑+________(没有配平)
(1)上述方程式中,缺项物质是________,配平方程式,并在下面补全反应物系数。
 NaClO2+
NaClO2+ HCl—→
HCl—→
(2)该反应中氧化剂和还原剂的物质的量之比是________________________________________________________________________。
生成0.2 mol ClO2转移电子的物质的量为________ mol。
(3)ClO2对污水中的Fe2+、Mn2+、S2-和CN-等有明显的去除效果。某污水中含CN- a mg·L-1,现用ClO2将CN-氧化,只生成两种无毒气体。处理100 m3这种污水,至少需要ClO2________ mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
碳酸镁晶须是一种新型的吸波隐形材料中的增强材料。
(1)合成该物质的步骤如下:
步骤1:配制0.5 mol·L-1 MgSO4溶液和0.5 mol·L-1 NH4HCO3溶液。
步骤2:用量筒量取500 mL NH4HCO3溶液于1 000 mL四口烧瓶中,开启搅拌器,温度控制在50 ℃。
步骤3:将250 mL MgSO4溶液逐滴加入NH4HCO3溶液中,1 min内滴加完后,用氨水调节溶液pH到9.5。
步骤4:放置1 h后,过滤,洗涤。
步骤5:在40 ℃的真空干燥箱中干燥10 h,得碳酸镁晶须产品(MgCO3·nH2O n=1~5)。
回答下列问题:
①步骤3中加氨水后的离子方程式_____________________________________________。
②步骤4为加快过滤速度,常用_________________________________________________(填过滤方法)。
(2)测定合成的MgCO3·nH2O中的n值。
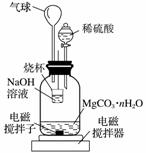
称量1.000 g碳酸镁晶须,放入右图所示的广口瓶中,加入适量水,滴入稀硫酸与晶须反应,生成的CO2被NaOH溶液吸收,在室温下反应4~5 h,反应后期将温度升到30 ℃,最后的烧杯中的溶液用已知浓度的盐酸滴定,测得CO2的总量;重复上述操作2次。
①图中气球的作用是______________________________________________________
__________________________;
②上述反应后期要升温到30 ℃,主要目的是__________________________________;
③设3次实验测得每1.000 g碳酸镁晶须产生的CO2平均值为a mol,则n值为________________________(用含a的表达式表示)。
(3)称取100 g上述晶须产品进行热重分析,热重曲线如下图。则该条件下合成的晶须中,n=____________(选填:1、2、3、4、5)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com