
| A.SF6易燃烧生成二氧化硫 | B.SF6中各原子均达到 8 电子稳定结构 |
| C.价层电子对数为6,正六面体结构 | D.SF6是由极性键构成的非极性分子 |
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③④ | B.①②③ | C.②③④ | D.①③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
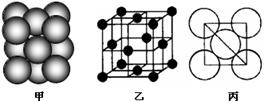
| | | | |||||||||||||||
| | | | | | A | | | | |||||||||
| | | B | | | C | | | ||||||||||
| | | | | | | D | E | | | | | | | | | | |
| 元 素 | D | E | |
| 电离能 /kJ·mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.离子晶体中可能含有共价键,但不一定含有金属元素 |
| B.分子晶体中一定含有共价键 |
| C.非极性分子中一定存在非极性键 |
| D.对于组成结构相似的分子晶体,一定是相对分子质量越大,熔沸点越高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 经催化剂作用变成N2和CO
经催化剂作用变成N2和CO 2,此反应中三种元素第一电离能由小到大的顺序为 ,在这四种物质中含有极性键的非极分子内
2,此反应中三种元素第一电离能由小到大的顺序为 ,在这四种物质中含有极性键的非极分子内 键和
键和 键的比为 。
键的比为 。| A.氢键 | B.离子键 | C.共价键 | D.配位键[E.范德华力 |
 对,则[Cu(NH3)n]+中n的值为
对,则[Cu(NH3)n]+中n的值为  。
。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.分子中 N-Cl键是非极性键 | B.分子中不存在孤对电子 |
| C.三氯化氮分子结构呈三角锥形 | D.因N-Cl 键键能大,它的沸点高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.从CH4、NH4+、SO42-为正四面体结构,可推测PH4+、PO43-也为正四面体结构 |
| B.NaCl与CsCl化学式相似,故NaCl与CsCl的晶体结构也相似 |
| C.苯不能使酸性高锰酸钾溶液褪色,故苯的同系物也不能使酸性高锰酸钾溶液褪色 |
| D.CO2通入Ca(ClO)2溶液生成CaCO3和HClO,SO2通入Ca(ClO)2溶液也生成CaSO3和HClO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com